海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验: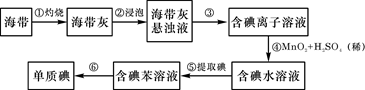
请填写下列空白:
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是 (从下列仪器中选出所需的仪器,用标号字母填写在空白处)。
| A.烧杯 | B.坩埚 | C.表面皿 | D.泥三角 E.酒精灯 F.干燥器 |
(2)步骤③的实验操作名称是 ;步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是 。
(3)步骤④反应的离子方程式是 。
(4)步骤⑤的实验操作名称是 ;某学生选择用苯来提取碘的理由是 。
(5)请设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法: 。
(8分)为了探究铁与氯气反应制取氯化铁的实验,某同学甲设计了如下的实验方案。其实验装置如下图,加热装置省略。已知:氯化铁易溶于水,熔、沸点低,受热易变为气态,而遇冷又易变为固态。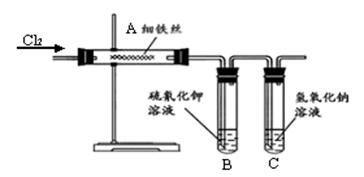
(1) 试管B中的现象是___________________,
试管B中的现象是___________________,
反应的离子方程式:_____________________________。
(2)试管C中氢氧化钠溶液的作用___________________________________。
(3)某同学乙猜测铁与氯气反应可能还会生成氯化亚铁,为了探究生成物中是否含有氯化亚铁(假设铁已完全反应),请你设计实验方案
(4)氯化铁易溶于水,熔、沸点低,受热易变为气态,而遇冷又易变为固态,故认为甲同学上述实验装置有缺陷。你认为丙同学判断的依据是: 。
(8分)实验室用氯化钠固体配制2.00mol·L-1的NaCl溶液220ml
(1)请补充该实验的实验步骤:
①计算,②称量,需要称量NaCl克,③溶解,④,⑤洗涤, ⑥,⑦ 摇匀。
(2)所需仪器为:容量瓶(规格:)、托盘天平、 烧杯,还需要那些玻璃仪器才能完成该实验,请写出: 。
。
(3)试分析下列操作对所配溶液的浓度有何影响。(填空:A---偏高、B---偏低、C---无影响,填序号)
①定容时,俯视液面。对所配溶液浓度的影响:
②定容后,加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度。对所配溶液浓度的影响 。
。
③配制前容量瓶用水洗涤后未 进行干燥处理__________。
进行干燥处理__________。
(9分)某学生设计了如下实验方法分离NaCl和CaCl2两种固体混合物。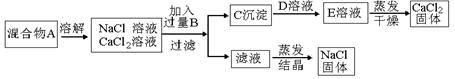
(1)B溶液是,加入过量B溶液的原因是,
反应的离 子方程式是。
子方程式是。
(2)经此实验方法分离得到的NaCl,经分析含有杂质,若要得到纯净的NaCl,还应补充的实验操作步骤是:
(3)若要测定该 混合物中NaCl和CaCl2的质量比,可称量干燥的C沉淀的质量(设为m1)和混合物A的质量(设为m2)来确定
混合物中NaCl和CaCl2的质量比,可称量干燥的C沉淀的质量(设为m1)和混合物A的质量(设为m2)来确定 ,混合物中NaCl和CaCl2的质量比为(用m1、m2表示)
,混合物中NaCl和CaCl2的质量比为(用m1、m2表示)
用98%的浓H2SO4(ρ=1.84g/cm3)配制 240mL0.5mol/L的稀H2SO4,请按要求填空:
(1)请写出该实验的实验步骤
①,②,③,④,⑤。
(2)所用浓H2SO4的物质的量浓度为 ,配制时所需浓硫酸的体积为mL。(均保留一位小数)
(3)实验中需要用到的定量仪器有(包括规格)
(4)若实验中出现下列 现象对所配溶液的浓度有什么影响?(填“偏高”、“偏低”或“无影响”)
现象对所配溶液的浓度有什么影响?(填“偏高”、“偏低”或“无影响”)
①浓硫酸溶解后未冷至室温即进行转移、定容。()
②定容时俯视刻度线。()
(5)若定容时液面高于刻度线应采取的措施是。
(6)若实验操作全部无误,最后所得的溶液应存放在试剂瓶中,并贴上标签,请你帮助把标签上的内容写一下(如右图)。
某同学应用如下所示装置研究物质的性质。其中气体C的主要成分是氯气,还含有少量空气和水蒸气。请回答下列问题: 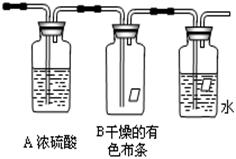
(1)该项研究的主要目的是_______。
(2)浓硫酸的作用是_______________。
(3)观察到的实验现象是___________________
(4)从物 质性质方面来看,这样的实验设计还存在事故隐患,事故表现在__。
质性质方面来看,这样的实验设计还存在事故隐患,事故表现在__。