(22分)在一固定容积的密闭容器中进行着如下反应:CO2(g) + H2(g) CO(g) + H2O(g) 其平衡常数K和温度t的关系如下:
CO(g) + H2O(g) 其平衡常数K和温度t的关系如下:
| t℃ |
700 |
800 |
850 |
1000 |
1200 |
| K |
2.6 |
1.7 |
1.0 |
0.9 |
0.6 |
(1) K的表达式为:_____ ____
____ _______________;
_______________;
(2) 该反应的正反应为 _______反应(“吸热”或“放热”);
(3) 能判断该反应是否已经达到化学平衡状态的是: ________
A.容器中压强不变 B.混合气体中CO浓度不变
C.v(H2)正 = v(H2O)逆 D.c(CO2) = c(CO)
(4)在850℃时,可逆反应:CO2(g) + H2(g)  CO(g) + H2O(g),在该容器内各物质的浓度变化如下:
CO(g) + H2O(g),在该容器内各物质的浓度变化如下:
| 时间/min |
CO2 (mol/L) |
H2 (mol/L) |
CO (mol/L) |
H2O( mol/L) mol/L) |
| 0 |
0.200 |
0.300 |
0 |
0 |
| 2 |
0.138 |
0.238 |
0.062 |
0.062 |
| 3 |
c1 |
c2 |
c3 |
c3 |
| 4 |
c1 |
c2 |
c3 |
c3 |
①前2min,用CO2表示该化学反应的速率是________________________________;
②在3-4mi n之间,反应处于_____________状态(填“平衡”或“非平衡”)。
n之间,反应处于_____________状态(填“平衡”或“非平衡”)。
③计算:3min—4min达到平衡时CO的平衡浓度c3和CO2 (g)的转化率,要求写出计算过程(850℃时,K值从上表可查出;c3精确到小数点后面三位数)。
(8分)下表列出了①~⑥六种元素在元素周期表中的位置。
 族 族周期 |
IA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
| 2 |
① |
② |
③ |
|||||
| 3 |
④ |
⑤ |
⑥ |
请回答下列问题:
(1) ①、②、③三种元素相比较,非金属性最强的是(填写元素符号);
(2) 元素②和⑥的氢化物中,稳定性较强的是(填氢化物的分子式);
(3) ①的最高价氧化物对应的水化物的化学式为 ;
(4)④、⑤两种元素的最高价氧化物对应的水化物在溶液中相互反应的离子方程式是
。
(8分)为提高人体素质, 避免人体缺碘影响正常的生命活动,我国早已采取食盐加碘措施。据报道, 人从食物中摄取碘后碘便在甲状腺中积存下来, 通过一系列化学反应可形成甲状腺素。甲状腺素的结构如下图,回答下列问题: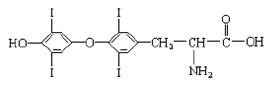
(1)甲状腺素由________种元素组成;
(2)“加碘食盐”中的碘元素以碘酸钾(KIO3 )的形式存在 , KIO3中碘的化合价是,我们用稀盐酸和淀粉KI试纸可以检验食盐中碘酸钾的存在,实验现象是。
(3)在“加碘食盐”包装袋上有“烹调时,待食品熟后加入碘盐” 文字说明,由此可推测碘酸钾在受热时容易。
(4分) 将钠在空气中燃烧,产物的化学式为 ;某无色气体与空气接触后,气体的颜色由无色变成红棕色,则原气体为 。
(6分) 在氮的单质和常见化合物中:
(1)常用作保护气(如填充灯泡、焊接保护等)的物质是;
(2)能与酸反应生成盐,在常温下为气态的物质是;
(3)在通常状况下是晶体,易溶于水,可以作氮肥,遇碱会放出带刺激性气味气体。写出它们与NaOH等强碱溶液反应的离子方程式。
【化学-有机化学基础】菠萝酯(结构简式如下)是一种具有菠萝香气的食用香料,
其的合成路线如下:
提示:
(1)有机物乙中所含有的官能团是_________
(2)上述合成菠萝酯的过程中,下列反应类型中未涉及到的是___________。
| A.取代反应 | B.加成反应 | C.消去反应 | D.中和反应 |
(3)菠萝酯有多种同分异构体,写出同时满足下列三个条件的同分异构体的结构简式。(写出其中的一种即可)
①能使溴的四氯化碳溶液褪色,遇FeCl3溶液不显紫色
②除苯环外无其他环状基团
③能与NaOH溶液反应,且1mol该同分异构体最多能与2molNaOH反应
_____________________________________________________________________
(4)写出由丙→菠萝酯的化学化学方程式。______________________________________。