'X、Y、Z均为短周期元素,它们在周期表中相对位置如图所示。若Y原子的最外层电子数是内层电子数的三倍,下列说法正确的是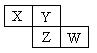
| A.X的气态氢化物比Y的稳定 |
| B.W的最高价氧化物对应水化物的酸性比Z的强 |
| C.Z的非金属性比Y的强 |
| D.X与Y形成的化合物都易溶于水 |
人体血液的pH为7.35~7.45,其中含有一对物质能抵御外来的少量酸或碱而保持pH基本稳定,这对物质可能是()
| A.NaCl-HCl | B.NaHCO3-H2CO3 |
| C.NaOH-HCl | D.Na2CO3-HCl |
反应A2+B2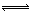 2AB在不同温度和压强改变条件下,产物AB的生成情况,如图所示:a为500℃,b为300℃时情况,c为300℃时从时间t3开始向容器中加压的情况,则下列叙述正确的是()
2AB在不同温度和压强改变条件下,产物AB的生成情况,如图所示:a为500℃,b为300℃时情况,c为300℃时从时间t3开始向容器中加压的情况,则下列叙述正确的是()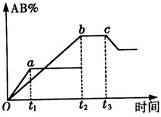
| A.A2、B2、AB均为气体,正反应放热 |
| B.AB为气体,A2、B2中最少有一种为非气体,正反应放热 |
| C.AB为气体,A2、B2中最少有一种为非气体,正反应吸热 |
| D.AB为固体,A2、B2中最少有一种为非气体,正反应吸热 |
在室温下,向饱和H2S溶液中缓慢通入过量SO2气体,溶液的pH值随通入SO2气体体积的变化曲线示意如图,合理的是()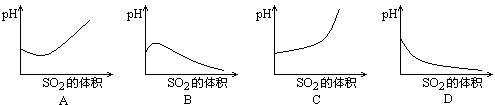
室温时,在水电离出c(H+)=1.0×10-14mol·L-1的溶液中,一定能大量共存的离子组是()
| A.K+、Na+、HCO3-、Cl- | B.K+、MnO4-、Br-、Cl- |
| C.Na+、Cl-、NO3-、SO42- | D.Al3+、NH4+、Cl-、SO42- |
强酸和强碱的稀溶液的中和热可表示为:
H+(aq)+OH-(aq)=H2O(1)△H =-57.3kJ/mol
已知:CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O△H ="-" Q1kJ/mol
1/2 H2SO4(浓) + NaOH(aq) ="=" 1/2Na2SO4(aq) +H2O(1)△H ="-" Q2kJ/mol
HNO3(aq)+KOH(aq)=KNO3(aq)+H2O(1)△H ="-" Q3kJ/mol
上述反应均为溶液中的反应,则Q1、Q2、Q3的绝对值大小的关系为( )
| A.Q1=Q2=Q3 | B.Q2>Q1>Q3 | C.Q2>Q3>Q1 | D.Q2=Q3>Q1 |