下列正确的叙述有( )
① CO2、NO2、P2O5均为酸性氧化物
② Ca(HCO3)2、Fe(OH)3、FeCl2均可由化合反应制得
③ 碘晶体分散到酒精中、氯化钠晶体分散到酒精中所形成的分散系分别为:溶液、胶体
④ 灼热的炭与CO2的反应、Ba(OH)2·8H2O与NH4Cl的反应均既属于氧化还原反应,又是吸热反应
⑤ 需要通电才可进行的有:电离、电解、电泳、电镀、电化腐蚀
⑥ 氯化铁溶液与氢氧化铁胶体具有的共同性质是:能透过滤纸,加热蒸干、灼烧后都有氧化铁生成⑦ 按照纯净物、混合物、强弱电解质和非电解质顺序排列的是单甘油酯、混甘油酯、苛性钾、次氯酸、氯气
⑧ 金属元素和非金属元素形成的化合物一定是离子化合物
| A.3个 | B.4个 | C.5个 | D.6个 |
下列变化需加入还原剂的是
A.HCO →CO2 →CO2 |
B.MnO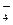 →Mn2+ →Mn2+ |
C.FeO→Fe3 O4 O4 |
D.Zn→Zn2+ |
恒温(1100℃)恒容密闭容器中发生反应:Na2SO4(s)+4H2(g)  Na2S(s)+4H2O(g)。下列说法正确的是
Na2S(s)+4H2O(g)。下列说法正确的是
| A.该反应的平衡常数表达式K=c(H2O)/c(H2) |
| B.若容器内气体的密度或压强保持不变,均说明该反应已达到平衡状态 |
| C.若Na2SO4足量,改变起始充入H2的浓度,达平衡时H2的转化率不变 |
| D.若初始时投入2.84gNa2SO4与一定量H2,反应达平衡时容器内固体共有2.264g,则Na2SO4的转化率为45% |
下列关于各溶液的描述中正确的是
| A.pH相等的①NH4Cl、②(NH4)2SO4、③NH4HSO4的溶液中,c(NH4+)大小:①=②>③ |
| B.常温下,在10mL pH=12的氢氧化钠溶液中加入pH=2的HA至pH刚好等于7,所得溶液体积V(总)≤20mL |
| C.向1.00L 0.3mol·L-1的NaOH溶液中缓慢通入CO2气体至溶液增重8.8g,所得溶液中: 3c(Na+)=2[c(HCO3-)+c(CO32-)+c(H2CO3)] |
| D.浓度均为0.1mol·L-1的CH3COOH和CH3COONa溶液等体积混合: |
c(CH3COO-)-c(CH3COOH)=c(H+)-c(OH-)
下列有关微粒性质的排序中,正确的是
| A.元素的非金属性:S>Cl>P>Si |
| B.元素第一电离能:O<N<F |
| C.离子半径:Al3+>Mg2+>Na+ |
| D.沸点:HCl<HBr<HF |
氯碱工业是一种高耗能产业,一种将燃料电池与电解池组合的新工艺可节能30%以上,下图是该工艺图示(电极未标出)。下列说法正确的是
| A.X为H2,Y这Cl2 |
| B.A池为电解池,且m<n |
| C.B池为燃料电池,且a<b |
| D.该工艺优点是燃料电池提供电能且能提高烧碱产品的浓度 |