化合物B是生活中一种常见的有机物,制取E和F的转化关系如下图所示。已知C能使溴水褪色,F有果香味。
(1)指出反应类型:① ;③ 。
(2)C的分子式为: 。
(3)写出②转化的化学方程式:② 。
(4)F有多种同分异构体,写出其中两种的结构简式 、 。
(9分)据报道,最近摩托罗拉(MOTOROLA)公司研发了一种由甲醇(CH3OH)和氧气以及强碱作电解质溶液的新型手机电池,电量可达现用镍氢或锂电池的十倍,可连续使用一个月才充一次电。据此请回答以下问题:
(1)甲醇是极,电极反应是;
(2)电池反应的离子方程式是;
(3)用该甲醇电池电解100 ml 0.4 mol/L的CuCl2溶液,当电池消耗0.3克甲醇时,电解池的阴极析出克(物质的化学式),若要恢复CuCl2溶液至原状,需加入克(填物质的化学式)。
(1)有四种一元酸HA、HB、HC、HD,相同物质的量浓度的NaD和NaB溶液的pH,前者比后者大,NaA溶液呈中性,1mol/L的KC溶液遇酚酞试液呈红色;同体积、同物质的量浓度的HB、HC用样的装置分别作导电性试验,发现后者的灯泡比前者亮,则这四种酸的酸性由强到弱的顺序为________________________。
(2)已知难溶电解质溶解平衡时M(OH)2(s) M2+(aq) +2OH— (aq),溶液的pH=a,则其Ksp=。
M2+(aq) +2OH— (aq),溶液的pH=a,则其Ksp=。
(3)溶液的酸度表示为AG=lg[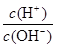 ],又知100℃时,水的离子积常数为1×10—12,25℃时纯水的AG1和100℃时食盐水的AG2的关系为:AG1AG2(=、<、>);在100℃时将V1ml AG=8的硫酸与V2ml AG=—6的烧碱溶液混合后AG=0,则V1:V2=。
],又知100℃时,水的离子积常数为1×10—12,25℃时纯水的AG1和100℃时食盐水的AG2的关系为:AG1AG2(=、<、>);在100℃时将V1ml AG=8的硫酸与V2ml AG=—6的烧碱溶液混合后AG=0,则V1:V2=。
(本题共11分,1分/空)
I、苯环上原有的取代基对新导入苯环上的取代基的位置有一定的影响,其规律是:①苯环上新导入的取代基所占的位置主要决定于原取代基的性质 。②可以把原取代基分成两类:第一类取代基,如—OH —Cl —Br —OCOR —R等,可使新导入的取代基进入苯环的邻位和对位;第二类取代基如—NO2,—SO3H,—CHO等可使新导入的取代基进入苯环的间位。现有如下图所示的转化关系:(每一步反应都只导入一个取代基)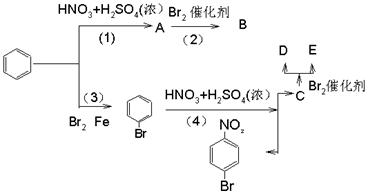
(1)写出A、B、C及同分异构体D、E的结构简式:A,B,C,D ,E 。
(2)写出图中(1)、(2)变化的化学方程式 、。
II、通常烷烃可以由相应的烯烃经催化加氢得到。但是,有一种烷烃A,分子式C9H20,它却不能由任何C9H18的烯烃催化加氢得到。而另有A的三个同分异构体B1、B2、B3,却分别可由而且只能由1种自己相应的烯烃催化加氢得到。A 、B1、B2、B3的结构简式如下(请填空)A, B1, B2, B3 。
(共7分,1分/空)本题以下几种物质是常用香精的主要成分(见右图):
(1)鉴别百里香酚和苏合香醇可采用的试剂为;
(2)苏合香醇能发生的有机反应类型有;(填序号)
A.加成反应 B.消去反应 C.加聚反应 D.取代反应
(3)写出符合下列条件的风信子醛的同分异构体的结构简式、;(任写二种)
a.含有苯环,苯环上有两个支链
b.与新制氢氧化铜悬浊液共热无砖红色沉淀
(4)已知醛在一定条件下可以两分子加成: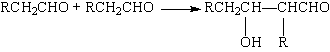
由枯茗醛合成兔耳草醛的路线如下:
①写出有机物A、B的结构简式、 。
②写出有机物C→兔耳草醛的化学方程式。
(本题共4分,1分/空)如下图所示,U型管的左端被水和胶塞封闭有甲烷和氯气(体积比为1:4)的混和气体,假定氯气在水中溶解度可以忽略。将封闭有甲烷和氯气的混和气体的装置放置在有光亮的地方,让混和气体缓慢的反应一段时间。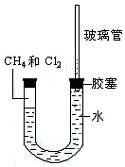
(1)假设甲烷与氯气反应充分,且只产生一种有机物,请写出化学
方程式。
(2)经过几个小时的反应后,U型管右端的玻璃管中水柱变化是。
A.升高 B.降低 C.不变 D.无法确定
(3)U型管左端的气柱变化是。
A.体积增大 B.体积减小 C.消失 D.不变
(4)试解释U型管右端的玻璃管中水柱变化的原因:____________。