20世纪30年代,Eyring和P elzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成,而是在反应物到生成物的过程中经过一个高能量的过渡态。
elzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成,而是在反应物到生成物的过程中经过一个高能量的过渡态。
⑴图I是HI分解反应中HI分子之间的几种碰撞示意图,其中属于有效碰撞的是______(选填“A”、“B”或“C”);
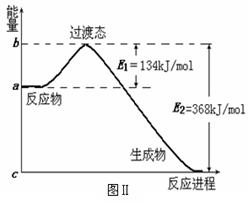
⑵图Ⅱ是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的
热化学方程式:____ __________________
__________________ _____________;
_____________;
⑶下表是部分化学键的键能数据:
| 化学键 |
P-P |
P-O |
O=O |
P=O |
| 键能/ kJ·mol–1 |
198 |
360 |
498 |
X |
已知白磷的燃烧热为2982kJ/mol,白磷(P4)、P4O6、P4O10结构如下图所示,
则上表中X=_______________。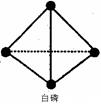

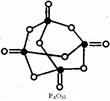
⑷0.5mol白磷(P4)与O2完全反应生成固态P4O6放出的热量为_________ __kJ。
__kJ。
A、B、C、D、E五种短周期元素,它们的原子序数依次增大;A是元素周期表中原子半径最小的元素;B元素最高价氧化物对应的水化物与其氢化物反应生成一种盐X;D与A同主族,且与E同周期;E元素原子的最外层电子数是其次外层电子数的=3/4倍;C与E同主族。
请回答下 列问题:
列问题:
(1)X的化学式为_____,D的原子结构示意图为_____。
(2)元素的非金属性C______ E(填“>”、“<”或“=”)。
下列各项中,能说明这一结论的事实有______(填序号)。
①氢化物H2E的酸性比H2C强
②氢化物H2C的热稳定性比H2E强
③氢化物H2E的水溶液放置在空气中会变浑浊
(3)BC和BC2气体可用纯碱溶液吸收,有关化学方程式为:
2 BC2+Na2CO3=NaBC2+NaBC3+CO2↑
BC+BC2+Na2CO3=2NaBC2+CO2↑
①配制1000g质量分数为21.2%的纯碱吸收液,需Na2CO3·10H2O多少克?
②现有1000g质量分数为21.2%的纯碱吸收液,吸收BC和BC2混合气体,每产生22.4L(标准状况)CO2时,吸收液质量增加44g。
(a)计算吸收液中NaBC2和NaBC3物质的量之比。
(b)1000g质量分数为21.2%的纯碱吸收液在20℃经充分吸收BC和BC2混合气体后,蒸发掉688g水,冷却到0℃,最多可析出NaBC2多少克?(0℃时,NaBC2的溶解度为71.2g /100g水)
亚氯酸钠(NaClO2)主要用于棉纺、造纸业的漂白剂,也用于食品消毒、水处理等,亚氯酸钠受热易分解。以 氯酸钠等为原料制备亚氯酸钠的工艺流程如下:
氯酸钠等为原料制备亚氯酸钠的工艺流程如下:
(1)提高“反应1”反应速率的措施有_________________、___________等。
(2)“反应2”的的氧化剂是_________,该反应的化学方程式为_____________。
(3)采取“减压蒸发”而不用“常压蒸发”,原因是______________________。
(4)从“母液”中可回收的主要物质是_________。
(5)“冷却结晶”后经______________(填操作名称)即可获得粗产品。
Ⅰ、氮元素是重要的非金属元素,可形成卤化物、氮化物,叠氮化物及配合物等多种化合物。
(1)NF3,NBr3、NCl3这三种分子的空间构型是 。
(2)叠氮酸(HN3)是一种弱酸,可部分电离出H+和N3-。请写出两种与N3-电子数相等的分子 。
(3)NaN3与KN3离子键强弱相比,NaN3 KN3(填“>”、“=”或“<” )。
(4)氮化碳结构如下图, 其硬度超过金刚石晶体,成为首屈一指的超硬新材料。
①写出氮化碳的化学式____ _ _____;
②指出氮化碳的晶体类型___________。
Ⅱ、分析表中四种物质的相关数 据,请回答:
据,请回答:
| CH4 |
SiH4 |
NH3 |
PH3 |
|
| 沸点/K |
101.7 |
161.2 |
239.7 |
185.4 |
| 分解温度/K |
873 |
773 |
1073 |
713.2 |
(1)CH4和SiH4比较,沸点高低的原因是___________;
(2)NH3和PH3比较,分 解温度高低的原因是___________;
解温度高低的原因是___________;
(3)结合上述数据和规律判 断,一定压强下HF和HCl的混合气体降温时___________先液化。
断,一定压强下HF和HCl的混合气体降温时___________先液化。
(15分)X、Y、Z、W是四种短周期元素,X原子的M层上的电子数是原子核外电子层数的2倍;Y原子最外层电子数是次外层电子数的2倍;2的最外层电子数与核外电子总数之比为5:7;W元素最高正价为+7价。
(1)元素W在周期表中的位置是_______________
(2)X、W两种元素的气态氢化物中,稳定性强的是_________(填化学式)
(3)在X2W2分子中,每个原子最外层均达到8电子稳定结构,则X2W2的电子式
为_______________.
(4)由Y2H6、O2、KOH溶液组成的燃料电池中。负极上发生的电极反应为___________________________.
(5)在碱性条件下,用W2将废水中的YZ-转化成Z2和YO32-等,从而使废水得到净化,则
其反应的离子方程式为__________________________________
(6)在常温下,0.2mol YX2(液态)在O2中完全燃烧,生成两种气态氧化物时放出的热量为215kJ,该反应的热化学方程式为_______________________________________.
(16分)(1)已知:还原性HSO3->I-,氧化性IO3->I2。在NaIO3溶液中滴加少量NaHSO3溶液,发生下列反应:NaIO3+NaHSO3→I2+Na2SO4+H2SO4+H2O
①配平上述反应的化学方程式(将化学计量数填在方框内);并写出其氧化产物____________。
②在NaIO3溶液中滴加过量NaHSO3溶液,反应完全后,推测反应后溶液中的还原产物为____________ (填化学式);
(2)向某密闭容器中加人0.15 mol/L A、0.05 mol/L C和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如下图中甲图所示[t0时c(B)未画出,t1时增大到0.05 mol/L]。乙图为t2时刻后改变反应条件,平衡体系中正、逆反应速率随时间变化的情况。
①若t4时改变的条件为减小压强,则B的起始物质的量浓度为________mol/L;
②若t1="15" s,则t0~t1阶段以C浓度变化表示的平均反应速率为v(C)=_______mol/(L·s)。
③t3时改变的某一反应条件可能是_______(选填序号)。
a使用 催化剂 b增大压强 c增大反应物浓度
催化剂 b增大压强 c增大反应物浓度
④有甲、乙两个容积均为2L的密闭容器,在控制两容器温度相同且恒定情况下,向甲中通入3mol A,达到平衡时,B的体积分数为20%,则向乙容器中充入1 mol C和0.5mol B,达到平衡时,C的浓度c(C)=________