反应物与生成物均为气态的某可逆反应在不同条件下的反应历程分别为A、B,如图所示。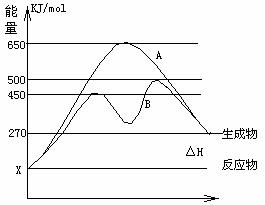
(1)据图判断该反应是___①___(填“吸”或“放”)热反应,当反应达到平衡后,其他条件不变,升高温度,反应物的转化率__②__ (填“增大”、“减小”或“不变”)
(2)其中B历程表明此反应采用的条件为___③___ (选填下列序号字母),作出正确的判断的理由为__④____
A、升高温度 B、增大反应物的浓度 C、降低温度 D、使用了催化剂
(3)若△H的数值为200KJ/mol,则此反应在A反应历程中的正反应的活化能为___⑤___KJ/mol,x值应为 ___⑥___KJ/mol
“低碳”在工业生产中意义重大,充分利用原材料,不排放或减少排放“三废”,不同工厂联合生产等都是很好的“低碳”生产方式。下面是几家工厂利用废气、废液、废渣联合生产化肥硫酸铵的工艺: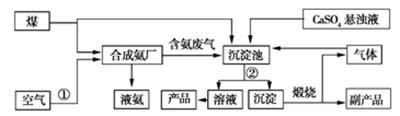
请回答下列问题:
(1)操作②为。
(2)工业合成氨的化学方程式为。
(3)沉淀池中生成硫酸铵的化学方程式为。
(4)在实验室中检验氨气的方法是。
(5)副产品的化学式为。该联合生产工艺中可以循环使用的物质是。
针对下面9种元素,完成以下各小题
| 周期 |
IA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
O |
| 2 |
① |
② |
③ |
|||||
| 3 |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
⑨ |
(1)单质为有色气体的元素是___________(填名称)。
(2)③与④⑤简单离子的半径由大到小的顺序为___________(填离子符号)。
(3)元素②的单质的电子式为__________。
(4)最高价氧化物对应的水化物酸性最强的是___________________。(填化学式)
(5)④和⑥的最高价氧化物对应的水化物反应的离子方程式为___________。
(6)⑦的单质的用途正确的是___________。
A.光导纤维 B.太阳能电池 C.普通玻璃 D.计算机芯片
(7)元素①和⑦非金属性较强的是____,写出一个能表示二者非金属性强弱关系的化学方程式为:__________。
钮扣电池的电极材料为Zn和Ag2O,电解质溶液为KOH,其电极反应为:
Zn + 2OH--2e- =" ZnO" + H2O Ag2O + H2O + 2e- =" 2Ag" + 2OH-
电池的负极是(填电极材料),正极发生的是反应(填反应类型),
总反应式为。
(共10分)用下列:①H2O ②H2O2③Ba(OH)2④Na2O2⑤Cl2⑥Ar⑦CO2等物质填空。 (1—4小题填序号)
(1)由离子键和非极性键构成的是
(2)由极性键和非极性键构成的是
(3)不存在化学键的是
(4)共价化合物有
(5)写出下列物质的电子式:Na2O2
绿原酸是一种新型高效的酚型天然抗氧化剂,在食品行业有着广泛的用途,在某些食品中可取代或部分取代目前常用的人工合成的抗氧化剂。
绿原酸
 +
+
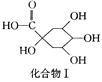
(1)在反应①中,绿原酸与水按1∶1发生反应,则绿原酸的分子式为。
(2)1 mol化合物Ⅰ与足量金属钠反应生成标准状况下氢气体积为。
(3)写出化合物Ⅱ与足量浓溴水反应的化学反应方程式:。
(4)1 mol化合物Ⅱ与足量的试剂X反应得到化合物Ⅲ(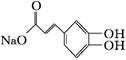 ),则试剂X是。
),则试剂X是。