(共10分)用下列:①H2O ②H2O2 ③Ba(OH)2 ④Na2O2 ⑤Cl2 ⑥Ar ⑦CO2 等物质填空。 (1—4小题填序号)
(1)由离子键和非极性键构成的是
(2)由极性键和非极性键构成的是
(3)不存在化学键的是
(4)共价化合物有
(5)写出下列物质的电子式:Na2O2
元素周期表中第四周期元素由于受3d电子的影响,性质的递变规律与短周期元素略有不同。
⑴第四周期过渡元素的明显特征是形成多种多样的配合物。
①CO可以和很多过渡金属形成配合物,如羰基铁[Fe(CO)5]、羰基镍[Ni(CO)4]。CO分子中C原子上有一对孤对电子,C、O原子都符合8电子稳定结构,CO的结构式为,与CO互为等电子体的离子为 (填化学式)。
②金属镍粉在CO气流中轻微加热,生成液态Ni(CO)4分子。423K时,Ni(CO)4分解为Ni和CO,从而制得高纯度的Ni粉。试推测Ni(CO)4易溶于下列。
a.水b.四氯化碳c.苯d.硫酸镍溶液
⑵第四周期元素的第一电离能随原子序数的增大,总趋势是逐渐增大的。镓的基态原子的电子排布式是,Ga的第一电离能却明显低于Zn,原因是。
⑶用价层电子对互斥理论预测H2Se和BBr3的立体结构,两个结论都正确的是。
a.直线形;三角锥形b.V形;三角锥形
c.直线形;平面三角形d.V形;平面三角形
⑷Fe、Co、Ni、Cu等金属能形成配合物与这些金属原子的电子层结构有关。
①Fe(CO)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)5晶体属于(填晶体类型)。
②CuSO4·5H2O(胆矾)中含有水合铜离子因而呈蓝色,写出胆矾晶体中水合铜离子的结构简式(必须将配位键表示出来)。
由氧化物经氯化作用生成氯化物是工业生产氯化物的常用方法,Cl2、CCl4是常用的氯化剂。如:
Na2O+Cl2=2NaCl+O2
CaO+Cl2=CaCl2+O2
SiO2+2CCl4=SiCl4+2COCl2
Cr2O3+3CCl4=2CrCl3+3COCl2
请回答下列问题:
⑴写出铬的原子结构示意图为与铬同周期的所有元素的基态原子中最外层电子数与铬原子相同的元素有____________(填元素符号),其中一种金属的晶胞结构如图所示,该晶胞中含有金属原子的数目为________。
⑵ CCl4分子中C原子采取杂化成键。
⑶ COCl2俗称光气,分子中C原子采取sp2杂化成键。光气分子的结构式是,其中碳氧原子之间共价键是(填序号)
a.2个σ键b.2个π键c.1个σ键、1个π键
⑷ CaO晶胞如右图所示,CaO晶体中Ca2+的配位数为。CaO晶体和NaCl晶体中离子排列方式相同,其晶格能分别为:CaO-3401kJ•mol-1、NaCl-786kJ•mol-1。导致两者晶格能差异的主要原因是。
下表是元素 周期表的一部分,请回答下列问题:(用元素符号或对应化学式回答问题)
周期表的一部分,请回答下列问题:(用元素符号或对应化学式回答问题)
| 族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
| 一 |
① |
||||||
| 二 |
② |
③ |
④ |
||||
| 三 |
⑤ |
⑥ |
⑦ |
⑧ |
⑨ |
⑩ |
⑴ ④⑤⑥的原子半径由大到小的顺序为
⑵ ②③⑦的最高价含氧酸的酸性由强到弱的顺序为
⑶ ⑦⑧⑨的第一电离能由小到大的顺序为
⑷比较④和⑨的氢化物的稳定性大小 ,沸点高低
,沸点高低
⑸写出元素⑩的 +1价含氧酸的结构式
+1价含氧酸的结构式
下表是长式周期表的一部分,其中的编号代表对应的元素。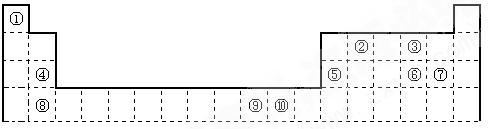
请回答下列问题:
(1)表中属于d区的元素是(填编号)。
(2)科学发现,②、④、⑨三种元素的原子形成的晶体具有超导性,其晶胞的结构特点如图(图中②、④、⑨分别位于 晶胞的体心、顶点、面心),则该化合物的化学式为(用对应的元素符号表示)。
晶胞的体心、顶点、面心),则该化合物的化学式为(用对应的元素符号表示)。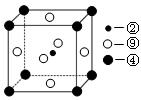
(3)元素②的一种氢化物是重要的化工原料,常把该氢化物的产量作为衡量石 油化工发展水平的标志。有关该氢化物分子的说法正确的是
油化工发展水平的标志。有关该氢化物分子的说法正确的是 。
。
a.分子中含有氢键 b.属于非极性分子
c.含有4个σ键和1个π键 d.该氢化物分子中,②原子采用sp2杂化
(4)某元素的外围电子排布式为nsnnpn+1,该元素可与①形成三角锥形的分子X, X在①与③形成的分子Y中的溶解度很大,其主要原因是
。
(5)将过量的X通入含有元素⑩的硫酸盐溶液中,现象是,反应的离子方程式_。
(6) ⑩单质晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示.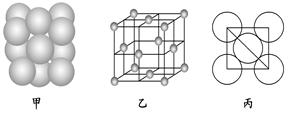
若已知⑩的原子半径为d,NA代表阿伏加德罗常数,⑩的相对原子质量为M,请回答:晶胞中⑩原子的配位数为________,该晶体的密度为________(用字母表示)。
有A、B、C、D、E五种短周期元素,它们的原子序数依次增大,其中B是地壳中含量最多的元素.已知A、C及B、E分别是同主族元素,且B、E两元素原子核内质子数之和是A、C两元素原子核内质子数之和的2倍.处于同周期的C、D、E元素中,D是该周期金属元素中金属性最弱的元素.
(1)试比较C 、D两元素最高价氧化物对应水化物碱性的强弱(填化学式)。
、D两元素最高价氧化物对应水化物碱性的强弱(填化学式)。
(2)A、B、C形成的化合物的晶体类型为,电子式为。
(3)写出D单质与C元素最高价氧化物对应水化物反应的离子方程式。
(4)写出两种均含A、B、C、E四种元素的化合物在溶液中相互反应、且生成气体的离子方程式。
(5)通常条件下, C的最高价氧化物对应水化物2mol与E最高价氧化物对应水化物1mol的稀溶液间反应放出的热量为114.6KJ,试写出表示该热量变化的热化学方程式。
(6)含有元素C的盐的焰色反应为________色.许多金属盐都可以发生焰色反应,其原因是_______________________ ________________________________.
________________________________.