山梨酸是一种常见的食物添加剂,它是一种无色针状晶体或白色粉末,它的结构简式为CH3—CH=CH—CH=CH—COOH。下列关于山梨酸的叙述不正确的是
| A.易溶于乙醇 | B.能与氢气发生加成反应 |
| C.能和乙醇反应生成酯 | D.1mol山梨酸能和金属钠反应生成1mol氢气 |
高温下,某反应达到平衡,平衡常数K=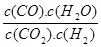 。恒容时,温度升高,H2浓度减小。下列说法正确的是
。恒容时,温度升高,H2浓度减小。下列说法正确的是
| A.该反应是焓变为正值 |
| B.恒温恒容下,增大压强,H2浓度一定减小 |
| C.升高温度,逆反应速率减小 |
D.该反应化学方程式为CO+H2O CO2+H2 CO2+H2 |
下列说法正确的是
| A.放热反应的焓变小于零,熵变大于零 |
| B.放热及熵增加的反应,一定能自发进行 |
| C.放热反应的焓变大于零,熵变小于零 |
| D.放热及熵减小的反应,一定能自发进行 |
在同温、同压下,下列各组热化学方程式中,△H1>△H2的是
| A.2H2O(g) = 2H2(g) + O2(g)△H1 2H2O(l) = 2H2(g) + O2(g)△H2 |
| B.S (g) + O 2(g) = SO2(g)△H1 S (s) + O 2(g) = SO2(g)△H2 |
| C.2C (s) + O 2(g) = 2CO (g)△H1 2C (s) + 2O 2(g) = 2CO2 (g)△H2 |
| D.H2(g) + Cl2(g) = 2HCl(g)△H1 |
2HCl(g) = H2(g) + Cl2(g)△H2
图1为某化学反应的速率与时间的关系示意图。下列有关t1时刻改变条件的说法正确的是
A.2SO2(g)+O2(g)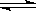 2SO3(g) ΔH<0,t1时刻升高温度 2SO3(g) ΔH<0,t1时刻升高温度 |
B.4NH3(g)+5O2(g)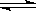 4NO(g)+6H2O(g) ΔH<0,t1时刻增大O2浓度 4NO(g)+6H2O(g) ΔH<0,t1时刻增大O2浓度 |
C.H2O(g)+CO(g)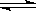 H2(g)+CO2(g) ΔH>0, t1时刻增大压强 H2(g)+CO2(g) ΔH>0, t1时刻增大压强 |
D.C(s)+H2O(g)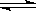 CO(g)+H2(g) ΔH>0,t1时刻升高温度 CO(g)+H2(g) ΔH>0,t1时刻升高温度 |
已知2NO2(g) N2O4(g),在体积都为V的A和B两个密闭玻璃容器中,分别注入容积颜色相同的NO2和Br2(气),然后将两个容器体积同时扩大为2V,过一会儿可以看到
N2O4(g),在体积都为V的A和B两个密闭玻璃容器中,分别注入容积颜色相同的NO2和Br2(气),然后将两个容器体积同时扩大为2V,过一会儿可以看到
A.A中颜色比B中浅 B.A中颜色比B中深
C.A、B中颜色深浅一样 D.A、B中颜色都比开始时深