下列有关反应热的叙述正确的是( )
| A.已知2H2(g)+O2(g)===2H2O(g);ΔH=-483.6kJ/mol,则氢气的燃烧热为241.8kJ/mol |
| B.C(石墨,s)===C(金刚石,s);ΔH>0,所以金刚石比石墨稳定 |
| C.已知碳的燃烧热为ykJ/mol,当7.2g的碳在12.8g的氧气中燃烧,至反应物耗尽并放出xkJ的热量,则可求出1mol碳与氧气反应生成一氧化碳时ΔH=(0.5y-2.5x)kJ/mol |
| D.己知2C(s)+2O2(g)===2CO2(g);ΔH1 2C(s)+O2(g)===2CO(g);ΔH2,则ΔH1>ΔH2 |
下列叙述错误的是( )
| A. 6Li和7Li的电子数相等,中子数也相等 |
| B.13C和14C属于同一种元素,它们互为同位素 |
| C.1H和2H是不同的核素,它们的质子数相等 |
| D.14C和14N的质量数相等,它们的中子数不等 |
下列关于钠的化合物的叙述中正确的是()
| A.Na2O和Na2O2都是白色固体 |
| B.Na2CO3能与石灰水反应而NaHCO3不反应 |
| C.Na2CO3受热后稳定性比NaHCO3强 |
| D.Na2O和Na2O2都能与水反应生成O2 |
奥运五环代表着全世界五大洲的人民团结在一起。下列各项中的物质,能满足如图中阴影部分关系的是( ) 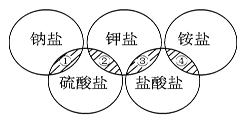
| ① |
② |
③ |
④ |
|
| A |
Na2SO4 |
K2SO4 |
KCl |
(NH4)2SO4 |
| B |
NaCl |
K2SO4 |
KCl |
NH4Cl |
| C |
Na2SO4 |
K2SO4 |
KCl |
NH4Cl |
| D |
NaCl |
K2SO4 |
KCl |
(NH4)2SO4 |
金属钠长期露置在空气中,最后转变为()
| A.Na2CO3 | B.Na2O2 | C.NaOH | D.Na2O |
通过对金属钠与水反应现象的观察,不能分析得出的结论是()
| A.金属钠熔点低 | B.金属钠导电性强 |
| C.金属钠密度小 | D.金属钠化学性质活泼[来源 |