针对苏教版化学I第75页上“铁与氧化性较弱的氧化剂(如盐酸、硫酸铜溶液等)反应转化为+2价铁的化合物,如果与氧化性较强的氧化剂(如氯气、双氧水等)反应则转化为+3价的化合物”的叙述,化学研究性学习小组拟通过以下实验探究“新制的还原性铁粉和盐酸的反应(铁过量)”。请你参与探究并回答有关问题: (1)通过简单的化学实验检验反应后混合物中的二价铁的实验方法和现象是 ;但在实验中往往又看到血红色迅速褪去,同时溶液呈黄色,其可能的原因是: ;学生在做实验时往往滴加双氧水的浓度过大,或者过量,还看到迅速产生大量气泡,写出产生该现象的化学方
(1)通过简单的化学实验检验反应后混合物中的二价铁的实验方法和现象是 ;但在实验中往往又看到血红色迅速褪去,同时溶液呈黄色,其可能的原因是: ;学生在做实验时往往滴加双氧水的浓度过大,或者过量,还看到迅速产生大量气泡,写出产生该现象的化学方 程式: 。
程式: 。 (2)有资料介绍“取少量反应液(含二价铁)先滴加少量新制饱和氯水,然后滴加KSCN溶液,呈现血红色。若再滴加过量新制氯水,却发现血红色褪去。同学对血红色褪去的原因提出各自的假
(2)有资料介绍“取少量反应液(含二价铁)先滴加少量新制饱和氯水,然后滴加KSCN溶液,呈现血红色。若再滴加过量新制氯水,却发现血红色褪去。同学对血红色褪去的原因提出各自的假 设。某同学的假设是:溶液中的+3价铁被氧化为更高的价态。”如果+3价铁被氧化为FeO42-,试写出该反应的离子方程式 。
设。某同学的假设是:溶液中的+3价铁被氧化为更高的价态。”如果+3价铁被氧化为FeO42-,试写出该反应的离子方程式 。 (3)探究高铁酸钾的某种性质。
(3)探究高铁酸钾的某种性质。 【实验1】将适量K2FeO4固体分别溶解于pH 为 4.74、7.00、11.50 的水溶液中,配得FeO42-浓度为 1.0 mmol·L-1(1 mmol·L—1 =10—3 mol·L—1)的试样,静置,考察不同初始 pH 的水溶液对K2FeO4某种性质的影响,结果见图1(注:800 min后,三种溶液中高铁酸钾的浓度不再改变)。
【实验1】将适量K2FeO4固体分别溶解于pH 为 4.74、7.00、11.50 的水溶液中,配得FeO42-浓度为 1.0 mmol·L-1(1 mmol·L—1 =10—3 mol·L—1)的试样,静置,考察不同初始 pH 的水溶液对K2FeO4某种性质的影响,结果见图1(注:800 min后,三种溶液中高铁酸钾的浓度不再改变)。

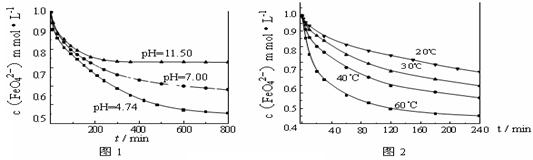

 【实验2】将适量 K2FeO4溶解于pH=4.74 的水溶液中,配制成FeO42-浓度为 1.0 mmol·L-1的试样,将试样分别置于 20℃、30℃、40℃和60℃的恒温水浴中,考察不同温度对K2FeO4某种性质的影响,结果见图2。则
【实验2】将适量 K2FeO4溶解于pH=4.74 的水溶液中,配制成FeO42-浓度为 1.0 mmol·L-1的试样,将试样分别置于 20℃、30℃、40℃和60℃的恒温水浴中,考察不同温度对K2FeO4某种性质的影响,结果见图2。则 ①实验1的目的是 ;
①实验1的目的是 ; ②实验2可得出的结论是 ;
②实验2可得出的结论是 ; ③高铁酸钾在水
③高铁酸钾在水 中的反应为4 FeO42—+10 H2O
中的反应为4 FeO42—+10 H2O 4 Fe(OH)3+8OH—+3 O2↑。由图1可知,800 min时,pH=11.50的溶液中高铁酸钾最终浓度比pH=4.74的溶液中高,主要原因是 。
4 Fe(OH)3+8OH—+3 O2↑。由图1可知,800 min时,pH=11.50的溶液中高铁酸钾最终浓度比pH=4.74的溶液中高,主要原因是 。
根据反应8NH3 + 3Cl2 == 6NH4Cl+ N2 ,回答下列问题:
6NH4Cl+ N2 ,回答下列问题:
(1) 还原剂是(写化学式);
(2) 用双线桥法表示该反应电子转移的方向和数目;
(3)当反应中转移1.806×1024个电子时,被氧化的气体在标准状况下的体积为升。
选择下列实验方法分离物质,将分离方法的序号填在横线上。
| A.萃取分液法 | B.结晶法 | C.分液法 | D.蒸馏法 E.过滤法 |
⑴分离饱和食盐水与沙子的混合物。
⑵分离水和汽油的混合物。
⑶分离四氯化碳(沸点为76.75℃)和甲苯的混合物(沸点为110.6℃)的混合物。
⑷从碘的水溶液里提取碘。
(10分)A、B代表不同物质,都是H、N、O、Na中的任意三种元素组成的强电解质,A的水溶液呈碱性,B的水溶液呈酸性,请找出A、B可能的两种组合。要求:相同浓度时,A1溶液中水的电离程度小于A2溶液中水的电离程度;相同浓度时,B1溶液中水的电离程度小于B2溶液中水的电离程度,且B2溶液中只有阳离子发生水解反应(已知:HNO2是弱酸)。
(1)写出化学式A1__________,A2_____ _____,B1__________,B2__________;
_____,B1__________,B2__________;
(2)相同温度下,当A1、B1的物质的量浓 度相等时,两溶液中水电离出的氢离子的物质的量浓度之比为________________________;
度相等时,两溶液中水电离出的氢离子的物质的量浓度之比为________________________;
(3)写出0.1  的
的 溶液中离子浓度大小排序________________;
溶液中离子浓度大小排序________________;
(10分)如下图所示,烧杯中都盛有稀硫酸。
(1)中反应的离子方程式为 ,
,
(2)中的电极反应:Fe:、Sn:
Sn极附近溶液的pH(填增大、减小或不变)
(3)中被腐蚀的金属是。
比较(1)、(2)、(3)中纯铁被腐蚀的速率由快到慢的顺序是(用序号回答)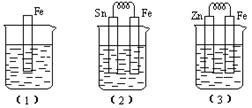
已知难溶于水的盐在水中存在溶解平衡:
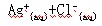
在一定温度下,水溶液中Ag+的物质的量浓度和Cl-的物质的量浓度的乘积为一常数,可用 KSP表示:KSP=c(Ag+) c(Cl-)=1.8·10-10
若把足量AgCl分别放入① 100 mL蒸馏水,② 100 mL 0.1 mol / L NaCl溶液,③ 100 mL 0.1 mol / L AlCl3溶液,④ 100 mL 0.1  mol / L MgCl2溶液中,搅拌后,在相同温度下Ag+浓度由大到小的顺序(用序号回答)是 ______ > ______ > ______ > ______。
mol / L MgCl2溶液中,搅拌后,在相同温度下Ag+浓度由大到小的顺序(用序号回答)是 ______ > ______ > ______ > ______。