下列各项比较中错误的是
| A.原子半径:Li<Na<K | B.酸性: H2SiO3 < H2CO3 < HNO3 < HClO4 |
| C.稳定性: SiH4 > H2S> HF | D.碱性: NaOH > Mg(OH)2 > Be (OH)2 |
根据下列数据确定元素X的相对原子质量。
(1) 1.01×105 Pa,273 ℃时气态单质Xn的密度为d g/L,则X的相对原子质量为_____。
(2)相同状况下,一定体积的X的气态氢化物HmX的质量是等体积NH3的2倍。则X的相对原子质量为_____。
(3)a个X原子的总质量为b g,则X的相对原子质量可表示为_____。
物质的量是高中化学中常用的物理量,请完成以下有关其内容的计算。
(1)0.2 g H2含有个______H原子。
(2)标准状况下,含有相同氧原子数的CO与CO2的体积之比为______。
(3)100 mL 某Al2(SO4)3溶液中,n(Al3+)="0.20" mol,则其中c(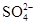 )= ______mol/L。
)= ______mol/L。
(4)在9.5 g某二价金属的氯化物中含0.2 mol Cl-,此氯化物的摩尔质量为______;该金属元素的相对原子质量为______。
(5)标准状况下6.72 L CO与一定量的 Fe2O3恰好完全反应(生成Fe和CO2)后,剩余固体的质量为______g。
CuSO4·5H2O是铜的重要化合物,有着广泛的应用。以下是CuSO4·5H2O的实验室制备流程图。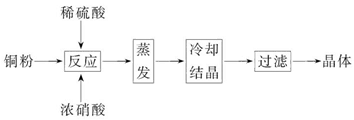
根据题意完成下列填空:
(1)向含铜粉的稀硫酸中滴加浓硝酸,在铜粉溶解时可以观察到的实验现象:_____________、_____________。
(2)如果铜粉、硫酸及硝酸都比较纯净,则制得的CuSO4·5H2O中可能存在的杂质是_____________,除去这种杂质的实验操作称为_____________。
(3)已知:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4。称取0.100 0 g提纯后的CuSO4·5H2O试样于锥形瓶中,加入0.100 0 mol/L氢氧化钠溶液28.00 mL,反应完全后,过量的氢氧化钠用
0.100 0 mol/L盐酸滴定至终点,耗用盐酸20.16 mL,则0.100 0 g该试样中含CuSO4·5H2O_____________g。
(4)上述滴定中,滴定管在注入盐酸之前,先用蒸馏水洗净,再用_____________。
孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物。以孔雀石为原料可制备CuSO4·5H2O及纳米材料G,步骤如下: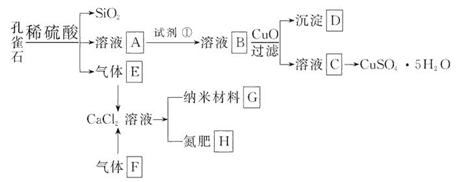
请回答下列问题:
(1)溶液A中的金属离子有Cu2+、Fe2+、Fe3+。从下列所给试剂中选择:实验步骤中,试剂①最佳为_______(填代号)。
a.KMnO4 b.(NH4)2S c.H2O2 d.HNO3
沉淀D中除了过量的CuO外,还存在另一种固体,其化学式为______________。加入CuO的作用是_____________________。
(2)由溶液C获得CuSO4·5H2O,需要经过一系列操作。除烧杯、漏斗外,过滤操作还用到另一玻璃仪器,该仪器在此操作中的主要作用是______________。
(3)制备纳米材料G时,应向CaCl2溶液中先通入(或先加入) _______ (填化学式)。写出该反应的化学方程式_______________________________________。
(4)欲测定溶液A中Fe2+的浓度,可用KMnO4标准溶液滴定,取用KMnO4标准溶液应用_______ (填写仪器名称);取A溶液稀释一定倍数后,用KMnO4标准溶液滴定,终点现象为_______。
离子反应是中学化学中重要的反应类型,回答下列问题:
(1)在发生离子反应的反应物或生成物中,一定存在________(填编号)。
①单质②氧化物③电解质④盐⑤化合物
(2)一种无色透明溶液中,可能含有下列离子: 、
、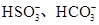 、I-和Cl-,取该溶液进行如下实验:
、I-和Cl-,取该溶液进行如下实验:
①将溶液滴在蓝色石蕊试纸上,呈红色。
②将少许溶液浓缩后加入铜片和硫酸,有无色气体析出,此气体通空气则立即变成红棕色。
③取少许溶液滴入BaCl2溶液,则产生白色沉淀。
④取实验③中的澄清溶液,滴入AgNO3试液,产生不溶于稀硝酸的白色沉淀。
⑤另取少许溶液,滴入NaOH溶液,有白色沉淀生成,当NaOH过量时,又有部分白色沉淀溶解。
根据以上现象判断,原溶液中肯定不存在的离子是_______;肯定存在的离子是_______;不能作出判断的离子是_______。