铅蓄电池的工作原理为Pb+PbO2+2H2SO4===2PbSO4+2H2O,研读下图,下列判断不正确的是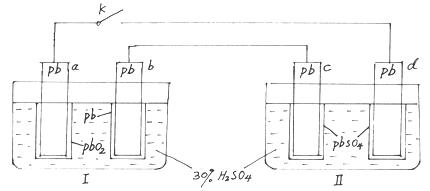
| A.K闭合时,d电极反应式:PbSO4+2H2O-2e-===PbO2+4H++SO42- |
| B.当电路中转移0.2 mol电子时,Ⅰ中消耗的H2SO4为0.2 mol |
| C.K闭合时,Ⅱ中SO42-向c电极迁移 |
| D.K闭合一段时间后,Ⅱ可单独作为原电池,d电极为正极 |
X、Y、Z、M代表四种金属元素,金属 X和Z用导线连接放入稀硫酸中时,X溶解,Z极上有氢气放出;若电解Y2+和Z2+共存的溶液时,Y先析出;又知M2+的氧化性强于Y2+。则这四种金属的活动性由强到弱的顺序为
X和Z用导线连接放入稀硫酸中时,X溶解,Z极上有氢气放出;若电解Y2+和Z2+共存的溶液时,Y先析出;又知M2+的氧化性强于Y2+。则这四种金属的活动性由强到弱的顺序为
| A.X>Z>Y>M | B.X>Y>Z>M | C.M>Z>X>Y | D.X>Z>M>Y |
原电池的正极和电解池的阴极所发生的反应分别是
| A.氧化、还原 | B.还原、氧化 |
| C.氧化、氧化 | D.还原、还原 |
在一定温度下,反应:2A(s)+2B(g) C(g)+D(g)在恒容容器中进行,不能说明该反应已经达到平衡的是
C(g)+D(g)在恒容容器中进行,不能说明该反应已经达到平衡的是
| A.容器内的压强不随时间而变化 | B.混合气体的密度不再随时间而变化 |
| C.A的质量不再改变 | D.平衡混合气体的平均相对分子质量不再改变 |
在恒温下的密闭容器中,有可逆反应2NO(气)+O2(气) 2NO2(气),不能说明已达到平衡状态的是
2NO2(气),不能说明已达到平衡状态的是
| A.正反应生成NO2的速率和逆反应生成O2的速率相等 |
| B.反应器中压强不随时间变化而变化 |
| C.混合气体颜色深浅保持不变 |
| D.混合气体平均分子量保持不变 |
盐酸倒在碳酸钙粉末上,能使反应的最初速率加快的是
| A.增加碳酸钙的用量 | B.盐酸浓度不变,使用量增加一倍 |
| C.盐酸浓度增加一倍,使用量减半 | D.盐酸浓度不变,使用量减半 |