如图所示装置:
①若烧杯中溶液为稀硫酸,
电极反应式为:正极 ;
负极 。
②若烧杯中溶液为氢氧化钠溶液,则负极为 ,
总反应方程为 。
(1)AgNO3的水溶液呈(填“酸”“中”或“碱”)性,原因是(用离子方程式表示):;实验室在配制AgNO3溶液时,常将AgNO3固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,以(填“促进”或“抑制”)其水解。
(2)明矾溶于水其中铝离子水解可用于净水,用离子方程式表示:
(3)纯碱可代替洗涤剂洗涤餐具,原因是(用离子方程式表示):
把NH4Cl晶体溶入水中,得到饱和NH4Cl溶液。若在该溶液中加入镁条, 观察到有产生,点燃有爆鸣声,此气体是,产生该气体的原因是(用离子方程式表示),微热后,能放出有刺激性气味的气体,它能使湿润的红色石蕊试纸变蓝,该气体是,产生该气体的原因是,总的离子反应方程式为。
一定温度下,有a.盐酸、b.硫酸、c.醋酸三种酸(用a、b、c回答)。
(1)当其物质的量浓度相同时。c(H+)由大到小的顺序是,pH由大到小的顺序是。
(2)同体积、同物质的量浓度的三种酸溶液,中和NaOH的能力由大到小的顺序是。
在①CH2===CH2,② ,③CH3CH2OH,④CH3COOH,⑤聚乙烯五种物质中:
,③CH3CH2OH,④CH3COOH,⑤聚乙烯五种物质中:
(1)能使Br2的CCl4溶液褪色的是________;
(2)属于高分子化合物的是________;
(3)能与Na2CO3溶液反应的是________;
(4)能发生酯化反应的是________;
(5)既能发生取代反应又能发生加成反应的是________。
在下列物质中是同系物的有________;互为同分异构体的有________,互为同素异形体的有________,互为同位素的有________,是同一种物质的有________。
(1)液氯(2)氯气(3)白磷(4)红磷(5)D (6)T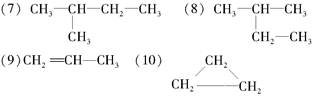
(11)2,2-二甲基丁烷