A是一种红棕色金属氧化物,B、D是金属单质,J是一种难溶于水的白色化合物,受热后容易发生分解。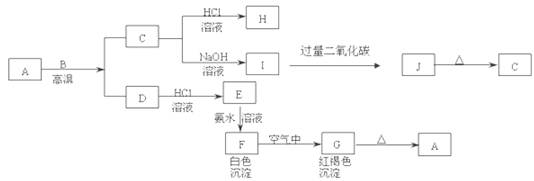
(1)写出下列物质的化学式:
A: E: J: G:
(2)按要求写方程式:
F在空气中转化为G的化学方程式: ;
C转化为I的离子方程式: ;
I转化为J的离子方程式: 。
【化学——选修2:化学与技术】
KMnO4是一种常用的强氧化剂,工业上以软锰矿(主要成分MnO2)为原料,通过液相法生产。即在反应器中碱性条件下用氧气氧化KnO2得到K2MnO4,分离后得到K2MnO4,再在电解槽中用铂板作用阳极,铁作阴极电解K2MnO4溶液得到KMnO4,简略生产过程如下所示: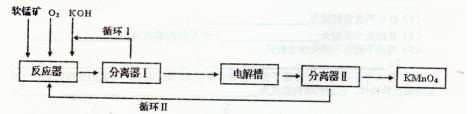
回答下列问题:
(1)写出反应器中反应的方程式_______
(2)生产过程中最好使用含MnO280%以上的富矿,因为MnO2含量较低的贫矿中Al的氧化物含量较高,会导致KOH消耗量偏离,用离子方程式表示KOH消耗偏高的原因____。
(3)写出电解槽中阴极和阳极的电极反应方程式阴极:_______ :阳极:____。
(4)在传统工艺中,得到K2MnO4后,向其溶液中避入CO2制备KMnO4,配平方程式:
K2MnO4+_______CO2=" _______KMnO4+_______" MnO2+ _______K2CO3
将所得到的KMnO4配成0.1mol·L-1KMnO4溶液,滴定20.00 rnL未知浓度的FeCl2液,消耗KMnO4溶液30.00 mL。滴定达到终点时的现象为:_______ ,则FeCl2溶液的浓度为_______mol/L。
在海底和青藏高原都发现了名为“可燃冰”的环保型新能源,主要成分是CH4,CH4在光照下可与Cl2反应,也可以用CH4和H2O为原料制备二甲醚和甲醇等新型燃料。
(1)CH4可与Cl2反应,其反应机理如下:
(2)Cl2→2Cl2 △H=" +243" kJ·mol-1
则CH4与Cl2反应生成CH3Cl(g)的热化学方程式为:________
(2)在一定条件下,发生反应:CH4(g)+H2O(g) ClO(g)+3H2(g)△H>0。
ClO(g)+3H2(g)△H>0。
在其它条件不变的情况下降低温度,逆反应速率将________(填“增大”、“减小”或“不变”)。若在2L密闭容器中发生反应,T℃时,通入2 mol CH4(g)和2 mol H2O(g),反应达平衡后,生成l mol CO,此时向容器中同时加入1mol CO和3 molH2的混合气体(保持温度不变),则平衡将_______(填“向正反应方向”、“向逆反应方向”或“不”)移动,达到新平衡后平衡常数_______
(3)CH4(g)和H2O(g)生成的CO和H2在一定条件下可发生反应CO(g)+2H2(g) CH3OH(g)△H=—90.1kJ·mol-1,恒容条件下达平衡,下列措施中能使n(CH3OH)/n(CO)增大的有________(选填序号)。
CH3OH(g)△H=—90.1kJ·mol-1,恒容条件下达平衡,下列措施中能使n(CH3OH)/n(CO)增大的有________(选填序号)。
a.再充入1 mol H2 b.使用健化剂 c.再充入2 mol CO d.升高温度
(4)CH4可用于设计燃料电池,甲烷燃料电池的工作原理如下图所示:则正极的电极反应式为________;反应一段时间后溶液的pH________(填“升高”、“降低”
或“不变”)。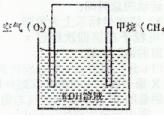
图中A~X分别代表一种反应物或生成物,其中F、G、X为单质,短周期元素X原予的核电荷数是其最外层和最内层电子数之和的3倍。已知A受热分解得到等物质的量的B、C、D三种气态物质,D气体能使湿润的红色石蕊试纸变蓝色,其它为化合物,图中部分生成物未列出。
请回答:
(1)B的电子式________,写出F的一种同素异形体____,D分子的空间构型为____。
(2)写出反应B与X反应的化学方程式________ 。
(3)写出A与足量K溶液加热时反应的离子方程式________。
(4)在一定条件下,2 L的H气体与0.5 L的G气体相混合,若该混合气体被NaOH溶液恰好完全吸收,只生成一种盐。请写出该反应过程中总的化学反应方程式:________。
(5)在F与J的反虚中当转移了1.5 mol电子时,产生标准状况下的I气体的体积为_______L。
(18分)以工业碳酸钙(含少量Na+、A13+、Fe3+等杂质)生产医用二水合氯化钙晶体(CaCl2·2H2O的质量分数为97.3—99.3%)的工艺流程为(可能用到的原子量Cl 35.5 Ca 40 O 16)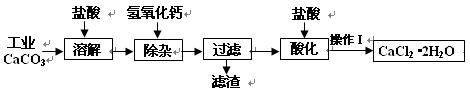
(1)CaCO3与盐酸反应的离子方程式。
(2)①加入氢氧化钙溶液调节溶液的PH为8.0—8.5,此时A13+、Fe3+沉淀完全,则滤渣主要成分的化学式为。
②过滤时需用的玻璃仪器除烧杯、玻璃棒外还有。
(3)酸化时加盐酸将溶液的PH调节到4.0左右,其目的为:
①,②防止Ca2+在蒸发时发生水解。
(4)操作Ⅰ中应包括、、过滤等实验步骤。
(5)为测定样品中CaCl2·2H2O的含量,称取0.735g样品配成250mL溶液,量取该溶液25.00mL于锥形瓶中,用0.05mol/L AgNO3溶液进行滴定,消耗AgNO3溶液的体积为20.40mL。
①通过计算,样品含CaCl2·2H2O的质量百分数为 .(只写计算式不计算结果)。
②若所测样品CaCl2·2H2O的质量百分数偏高(忽略其它实验操作误差),可能的原因之一为。
(1)大气中SO2含量过高会导致雨水中含有 (填化学式)而危害植物和建筑物。工厂排放的SO2尾气用饱和Na2SO3溶液吸收可得到重要化工原料NaHSO3,反应的化学方程式为。
(2)SO2是空气质量报告的指标之一,可用SO2还原KIO3生成I2的反应测定空气中SO2含量。每生成0.01mol I2,参加反应的SO2为 mol。
 (3)合成氨的反应N2(g)+3H2(g)
(3)合成氨的反应N2(g)+3H2(g)  2NH3(g) △H = -92.4 kJ·mol-1,一定条件下的密闭容器中,该反应达到平衡,要提高N2的转化率,可以采取的措施是__________(填字母代号)。
2NH3(g) △H = -92.4 kJ·mol-1,一定条件下的密闭容器中,该反应达到平衡,要提高N2的转化率,可以采取的措施是__________(填字母代号)。
a.升高温度b.加入催化剂 c.增加H2的浓度
d.增加N2的浓度e.分离出NH3  (4)在25℃下,向浓度均为0.1 mol·L-1的MgCL2和CuCl2混合溶液中逐滴加入氨水,先生成__________沉淀(填化学式),生成该沉淀的离子方程式为____________。已知25℃时Ksp[Mg(OH)2]=1.8×10-11,KsP[Cu(OH)2]=2.2×10-20。
(4)在25℃下,向浓度均为0.1 mol·L-1的MgCL2和CuCl2混合溶液中逐滴加入氨水,先生成__________沉淀(填化学式),生成该沉淀的离子方程式为____________。已知25℃时Ksp[Mg(OH)2]=1.8×10-11,KsP[Cu(OH)2]=2.2×10-20。 (5)在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应后溶液中c(NH4+)=c(Cl-),则溶液显_____________性(填“酸”“碱”或“中”), 可推断a 0.01(填大于、等于或小于)。
(5)在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应后溶液中c(NH4+)=c(Cl-),则溶液显_____________性(填“酸”“碱”或“中”), 可推断a 0.01(填大于、等于或小于)。