2SO2(g)+O2(g) =2SO3(g)反应过程的能量变化如图所示。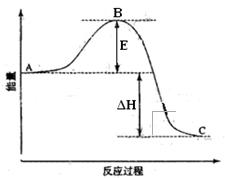
已知1mol SO2(g)氧化为1mol SO3的ΔH=-99kJ·mol-1.请回答下列问题:
(1)图中A、C分别表示 、 ,
(2)图中△H= KJ·mol-1;
(3)已知单质硫的燃烧热为296 KJ·mol-1,计算由S(s)生成3 molSO3(g)的△H (要求计算过程)。
有两个密闭容器A和B,A容器内有一个移动的活塞能使容器内保持恒压,B容器能保持恒容。
起始时向这两个容器中分别充入等量的体积比为2:1的SO2和O2的混合气体,并使A和B的容积相等。在保持4000C的条件下使之发生如下反应:2 SO2+O2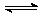 2SO3。
2SO3。
(1)达到平衡时所需要的时间A容器比B容器,A容器中SO2的转化率比B容器。
(2)达到(1)所述平衡后,若向两容器中通入数量不多的等量氩气,A容器化学平衡移动,B容器化学平衡 移动。
移动。
(3 )达到(1)所述平衡后,若向两容器中通入等量的原反应气体,达到平衡时,A容器SO3物质的量分数;B容器中SO3的物质的量分数。(填增大、减小、不变)
)达到(1)所述平衡后,若向两容器中通入等量的原反应气体,达到平衡时,A容器SO3物质的量分数;B容器中SO3的物质的量分数。(填增大、减小、不变)
在一定条件下,xA + yB zC,反应达到平衡,试填写下列空白:
zC,反应达到平衡,试填写下列空白:
(1)若A、B、C都是气体,减压后向逆反应方向移动,则x、y、x之间的关系是。
(2)已知C是气体,且x+y=z,加压时平衡如果发生移动,则平衡必向方向移动,且A、B的状态中至少有一种是。
(3)加热后C的百分含量减少,则正反应是反应(选填“吸热”、“放热”)。
今有a.盐酸 b.硫酸 c.醋酸三种酸,回答下列问题。(用酸的序号填写)
(1)在同体积、同浓度的三种酸中,分别加入足量的锌粒,在相同条件下产生H2的体积由大到小的顺序是_________________;
(2)在同体积、同pH的三种酸中,分别加入足量的锌粒,在相同条件下产生H2的体积由大到小的顺序是_______________;
(3)物质的量浓度均为0.1 mol·L-1的三种酸溶液的pH由大到小的顺序是___________ 。 如果取等体积的0.1 mol·L-1的三种酸溶液,用0.1 mol·L-1的NaOH溶液中和,当恰好完全反应时,消耗NaOH溶液的体积由大到小的顺序是______________。
。 如果取等体积的0.1 mol·L-1的三种酸溶液,用0.1 mol·L-1的NaOH溶液中和,当恰好完全反应时,消耗NaOH溶液的体积由大到小的顺序是______________。
现有下列物质 ①NaCl晶体 ②液态SO2③纯醋酸 ④硫酸钡 ⑤铜 ⑥酒精(C2H5OH)⑦熔化的KCl⑧NaOH溶液
请用以上物质回答下列问题。(填序号)
(1)属于强电解质且在上述状态下能导电的是;
(2)属于弱电解质的是;
(3)属于非电解质,但溶于水后的水溶液能导电的是。
7分)某温度(t℃)时,水的KW=1×10-13,则该温度(填大于、等于或小于)25℃,理由是。
将此温度下pH=11的NaOH溶液aL与pH=1的H2SO4溶液bL混合,
(1)若所得混合溶液为中性,则a:b=;
(2)若所得混合溶液pH=2,则a:b=。