[化学一有机化学基础](13分)对羟基扁桃酸是合成香料的重要中间体,它可由如下反应合成: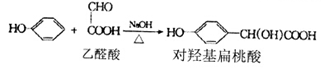
已知:
没有 —氢的醛与强碱共热时,该醛一分子被氧化成酸,另一分子被还原成醇的反应称为康尼查罗(Cnanizzoar)反应。如:2HCHO+NaOH
—氢的醛与强碱共热时,该醛一分子被氧化成酸,另一分子被还原成醇的反应称为康尼查罗(Cnanizzoar)反应。如:2HCHO+NaOH  CH3OH+HCOONa
CH3OH+HCOONa
(1)对羟基扁桃酸的分子式______________,乙醛酸分子中一种含氧官能团的名称________。
(2)写出一种满足下列三个条件的对羟基扁桃酸的同分异构体结构简式________________。
a.属于甲酸酯 b.含酚羟基 c.含亚甲基(一CH2一)
(3)苯酚能与甲醛发生聚合反应生成酚醛树脂,写出酚醛树脂的结构简式________________。
(4)对羟基扁桃酸不能发生的反应类型有_____________________________(填选项)。
| A.加成 | B.消去 | C.加聚 | D.取代 |
(5)写出乙醛酸发生康尼查罗反应的化学方程式_____________________________________.
在下列事实中,什么因素影响了化学反应速率:
(1)集气瓶中H2和Cl2的混合气体,在瓶外点燃镁条时发生爆炸:_____________________。
(2)熔化的KClO3放出气泡很慢,撒入少量MnO2很快产生气体:_____________________。
(3)同浓度、同体积的盐酸中分别放入同样大小的锌粒和镁条,产生气体有快有慢:_______。
(4)夏天的食品易霉变,而冬天不易发生该现象:_______________________
某温度时,在1L密闭容器中,A、B、C三种气态物质的物质的量随时间变化的曲线如图所示。由图中数据分析:
(1)该反应的化学方程式: ;
(2)反应开始至2min末,A的反应速率为 ;
(3)该反应是由 开始进行的。填序号
①正反应 ②逆反应 ③正逆反应同时
(1)如果反应物所具有的总能量大于生成物所具有的总能量,反应物转化为生成物时 (填吸收或放出)热量,△ H (填大于或小于)0;
(2)对于反应2SO2 + O2 2SO3其它条件不变,只改变一个反应条件,将生成SO3的反应速率的变化填入表中空格里 。(填字母 A.增大 B.减小 C.不变)
2SO3其它条件不变,只改变一个反应条件,将生成SO3的反应速率的变化填入表中空格里 。(填字母 A.增大 B.减小 C.不变)
| 改变条件 |
速率变化 |
||
| 降低温度 |
|
||
| 增大O2的浓度 |
|||
| 使用V2O5做催化剂 |
|||
| 压缩气体 |
已知A、B、C、D为第三周期元素,其原子的第一至第四电离能如下表所示:(单位:kJ/mol),回答下面各题:
| 元素代号 |
I1 |
I2 |
I3 |
I4 |
| A |
2080 |
4000 |
6100 |
9400 |
| B |
500 |
4600 |
6900 |
9500 |
| C |
740 |
1500 |
7700 |
10500 |
| D |
580 |
1800 |
2700 |
11600 |
(1)A是 B是 C是 D是 (填元素符号)
(2)B通常显 价,B的电负性 C的电负性(填“>”、“<”或“=”)。
(3)元素C的第一电离能比D高的原因是___________________________
(4)下列元素中,化学性质和物理性质最像A元素的是 。
A.氦(1s2) B. 铍(1s22s2) C. 锂(1s22s1) D. 氢(1s1)
(5)每种元素都出现相邻两个电离能的数据相差较大的情况,请你估计B的第2次电离能飞跃数据将是第___电子。
氮化硅是一种高温陶瓷材料,它的硬度大、熔点高、化学性质稳定。工业上普遍采用高纯硅与纯氮在1300℃反应获得氮化硅。
(1)根据性质,推测氮化硅属于________晶体。
(2)根据化合价规律,推测氮化硅的化学式为_________。
(3)现用四氯化硅和氮气、氢气加强热反应,可得较高纯度的氮化硅,反应的化学方程式为______ ___________。