某溶液中可能含有大量的Mg2+、Al3+、H+、Cl—和少量OH—,向该溶液中逐滴加入0.5mol·L—1NaOH溶液,生成沉淀的质量和加入NaOH溶液的体积之间的关系如下图所示,则可判断原溶液中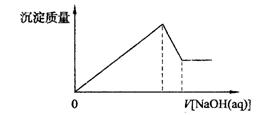
| A.有Mg2+,没有Al3+ |
| B.有Al3+,没有Mg2+ |
| C.有Mg2+和Al3+ |
| D.有大量的H+、Mg2+和Al3+ |
国庆期间对天安门广场大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开。S-诱抗素的分子结构如图,下列关于该物质的说法正确的是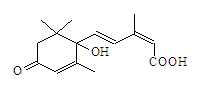
| A.其分子式为C15H18O4 |
| B.1mol该物质与NaOH溶液反应,最多可消耗2mol NaOH |
| C.既能发生加成反应,又能发生取代反应和消去反应 |
| D.既能与FeCl3溶液发生显色反应,又能使酸性KMnO4溶液褪色 |
下列有关说法正确的是
| A.铁表面镀铜时,铜与电源的正极相连,铁与电源的负极相连 |
| B.用pH均为2的盐酸和醋酸分别中和等物质的量的NaOH,消耗醋酸的体积更大 |
| C.一定温度下,反应2Mg(s)+CO2(g)=2MgO(s)+C(s)能自发进行,则该反应△H<0 |
D.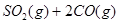  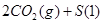 达到平衡,保持其他条件不变,分离出硫,正反应速率加快,SO2的转化率提高 达到平衡,保持其他条件不变,分离出硫,正反应速率加快,SO2的转化率提高 |
短周期主族元素A、B、C、D、E的原子序数依次增大,其中只有C是金属元素,B是地壳中含量最多的元素,A元素常见化合价为+1和-1;A与C的最外层电子数相同,C、D两元素原子的电子数之和为A、B两种元素原子的电子数之和的3倍。下列叙述正确的是
A.元素的原子半径:A<B<C<D< E
B.对应氢化物的热稳定性:D > E
C.B与C、B与D形成的化合物中化学键类型相同
D.五种元素中最高价氧化物对应的水化物酸性最强的是E
Mg-H2O2电池可用于驱动无人驾驶的潜航器。该电池以海 水为电解质溶液,示意图如下。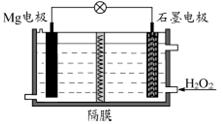
该电池工作时,下列说法不正确的是
| A.Mg电极是该电池的负极 |
| B.H2O2在石墨电极上发生还原反应 |
| C.石墨电极附近溶液的pH增大 |
| D.溶液中Cl-向正极移动 |
下列表示对应化学反应的离子方程式正确的是
A.向氯化铝溶液通入过量的氨气:Al3+ +4OH- AlO2- +2H2O AlO2- +2H2O |
B.过量氯气通人溴化亚铁溶液中2Cl2 +2Fe2+ +2Br- 4Cl-+2Fe3++ Br2 4Cl-+2Fe3++ Br2 |
| C.次氯酸钠与浓盐酸反应产生Cl2:ClO-+Cl—+H2O=Cl2↑+2OH— |
| D.NaHCO3溶液与少量Ba(OH)2溶液反应:Ba2++2OH-+2HCO3-=BaCO3↓+CO32—+2H2O |