已知:H2(g)+F2(g)=2HF(g) △H=—270kJ/mol,下列说法正确的是( )
| A.2L氟化氢气体分解成1L的氢气和1L的氟气吸收270kJ热量 |
| B.1mol氢气与1mol氟气反应生成2mol液态氟化氢放出的热量小于270kJ |
| C.在相同条件下,1mol氢气与1mol氟气的能量总和大于2mol氟化氢气体的能量 |
| D.1个氢气分子与1个氟气分子反应生成2个氟化氢分子放出270kJ热量 |
下图中每条折线表示周期表ⅣA~ⅦA族中的某一族元素氢化物的沸点变化,每个小黑点代表一种氢化物,其中a点代表的是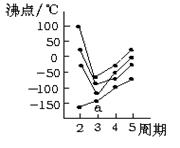
| A.H2S | B.HCl | C.SiH4 | D.PH3 |
在理论上不能用于设计原电池的化学反应是
| A.2FeCl3(aq)+2KI(aq) = 2FeCl2(aq)+2KCl(aq)+I2(aq)△H <0 |
| B.Ba(OH)2·8H2O(s)+2NH4Cl(s) = BaCl2(aq)+2NH3·H2O(aq)+8H2O(1)△H >0 |
| C.4Al(s)+ 6H2O(1)+ 3O2(g)==4Al(OH)3(s)△H <0 |
| D.Zn(s)+2MnO2(s)+2H2O(1) = 2MnOOH(s) +Zn(OH)2(s)△H <0 |
下列说法正确的是
| A.同温同压下,H2 + Cl2 = 2HCl在光照和点燃条件的△H不同 |
| B.铅蓄电池在放电过程中,负极质量减小,正极质量增加 |
| C.天然气、沼气和水煤气分别属于化石能源、可再生能源和一级能源 |
| D.元素原子的核外电子排布呈周期性变化是元素性质呈现周期性变化的根本原因 |
下列化学用语正确的是
A.硫原子的原子结构示意图: |
B.过氧化钠的电子式:Na+[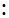 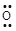 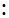 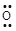 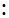 ]2-Na+ ]2-Na+ |
C.原子核内有8个质子、10个中子的氧原子: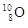 |
| D.HClO的结构式为 H—Cl—O |
2014年是门捷列夫诞辰180周年,下列事实不能用元素周期律解释的只有
| A.相对原子质量:Ar > K | B.碱性:KOH > NaOH |
| C.酸性:HClO4 > H2SO4 | D.元素的金属性:Mg > Al |