关于强、弱电解质的叙述不正确的是( )
| A.强电解质在溶液中完全电离,不存在电离平衡 |
| B.同一弱电解质溶液,温度不同时,导电能力不同 |
| C.强电解质溶液导电能力一定很强,弱电解质溶液导电能力一定很弱 |
| D.强电解质在固态或液态时,可能不导电 |
某原电池总反应离子方程式为2Fe3++Fe====3Fe2+,能实现该反应的原电池是()
| A.正极为Cu,负极为Fe,电解质溶液为FeCl3溶液 |
| B.正极为Cu,负极为Fe,电解质溶液为Fe(NO3)2溶液 |
| C.正极为Fe,负极为Zn,电解质溶液为Fe2(SO4)3溶液 |
| D.正极为Ag,负极为Fe,电解质溶液为CuSO4溶液 |
如下图所示的装置,在铁圈和银圈的焊接处,用一根棉线将其悬吊在盛水的烧杯中,使之平衡。小心地向烧杯中央滴入CuSO4溶液,片刻后可观察到的现象是()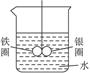
| A.铁圈和银圈左右摇摆不定 | B.保持平衡状况 |
| C.铁圈向下倾斜 | D.银圈向下倾斜 |
下列关于电解法精炼粗铜的叙述中不正确的是()
| A.粗铜板作阳极 |
| B.电解时,阳极发生氧化反应,而阴极发生的反应为:Cu2++2e-====Cu |
| C.粗铜中所含Ni、Fe、Zn等金属杂质,电解后以单质形式沉积槽底,形成阳极泥 |
| D.电解铜的纯度可达 99.95%—99.98% |
随着人们生活质量的不断提高,废电池必须进行集中处理的问题被提到议事日程,其首要原因是()
| A.利用电池外壳的金属材料 |
| B.防止电池中汞、镉和铅等重金属离子对土壤和水源的污染 |
| C.不使电池中渗漏的电解液腐蚀其他物品 |
| D.回收其中的石墨电极 |
镍镉(Ni-Cd)可充电电池可以发生如下反应:
Cd(OH)2+2Ni(OH)2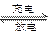 Cd+2NiO(OH)+2H2O。由此可见,该电池的负极材料是()
Cd+2NiO(OH)+2H2O。由此可见,该电池的负极材料是()
| A.Cd | B.NiO(OH) | C.Cd(OH)2 | D.Ni(OH)2 |