设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.标准状况下,22.4L异丁烷中含有的甲基数为2NA |
| B.168g NaHCO3固体中含离子总数为6 NA |
| C.46g乙醇中含C—H键总数为5NA |
D.含NA个Na+的Na2O溶解于1L水中,Na+的物质的量浓度为0.5 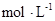 |
下列化学式能真实表示物质分子组成的是
| A.NaOH | B.CO2 | C.C | D.SiO2 |
下列实验事实,不能证明苯分子中的碳碳键不是单、双键交替,而是一种介于碳碳单键与碳碳双键之间的特殊的共价键的是
| A.苯不能使酸性高锰酸钾溶液褪色 | B.苯的邻二氯取代产物只有一种 |
| C.苯不使溴的四氯化碳溶液褪色 | D.苯的对二氯取代产物只有一种 |
下列关于同系物的叙述不正确的是
| A.同系物官能团的种类与个数必须相同 |
| B.相邻两个同系物的相对分子质量相差14 |
| C.通式相同的有机物一定互为同系物 |
| D.同系物具有相似的化学性质 |
从结构上分析推测,CH2=CHCOOCH2CH3,最不可能具有的性质是
| A.能使溴水褪色 | B.能使酸性高锰酸钾溶液褪色 |
| C.能水解 | D.能够与Na2CO3溶液反应 |
用括号内的物质除去试剂中少量的杂质,正确的是
| A.乙烷中的乙烯(氢气) | B.乙酸乙酯中的乙酸(饱和Na2CO3) |
| C.溴苯中的溴(苯) | D.乙烯中的SO2(KMnO4溶液) |