分析如图所示的四个原电池装置,其中结论正确的是 ( )
| A.①②中Mg作为负极,③④中Fe作为负极 |
| B.②中Mg作为正极,电极反应式为6H2O+6e-===6OH-+3H2↑ |
| C.③中Fe作为负极,电极反应为Fe-2e-===Fe2+ |
| D.④中Cu作为正极,电极反应式为2H++2e-===H2↑ |
【改编】25℃时,0.1mol/LNa2CO3溶液pH=12,下列判断正确的是
A.通入少量HCl气体后溶液中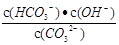 增大 增大 |
| B.升高温度溶液中c(OH-)和c(CO32-)均增大 |
| C.2c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3) |
| D.c(HCO3-)+c(H+)+2c(H2CO3)=0.01mol/L |
某小组为研究电化学原理,设计了下图所示的电化学装置,电极I为锌,其他电极均为石墨,盐桥是浸泡了饱和氯化钾溶液的琼脂,丙池是滴加了酚酞的氯化钠溶液。下列叙述正确的是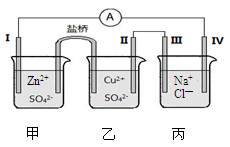
| A.电子由电极IV通过外电路流向电极I |
| B.装置工作过程中III电极周围出现红色 |
| C.电极II发生还原反应 |
| D.盐桥中Cl—向乙池移动 |
【原创】NA表示阿伏加德罗常数,下列叙述中正确的是
| A.室温下,31.0g白磷中含有的共价键数目为NA |
| B.3.6g过氧化钙(CaO2)固体中阴、阳离子总数约为0.1NA |
| C.60gSiO2中含有NA个SiO2分子 |
| D.1molFel2与足量氯气反应时转移的电子数为2NA |
下列表述正确的是
| A.氧化铁是一种碱性氧化物,常用作红色油漆和涂料 |
| B.在医疗上碳酸钠、氢氧化铝均可用于治疗胃酸过多 |
| C.Na2O2与水反应,红热的Fe与水蒸气反应均能生成碱 |
| D.人造刚玉熔点很高,可用作高级耐火材料,主要成分是SiO2 |
【原创】25℃时,下列各组离子在指定溶液中一定能大量共存的是
| A.pH=13的溶液中:Na+、K+、NO3-、S2‾ |
| B.能使氢氧化铝溶解的溶液:Na+、Mg2+、HCO3—、SO42‾ |
C.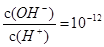 的溶液中:NH4+、K+、SiO32—、SO42‾ 的溶液中:NH4+、K+、SiO32—、SO42‾ |
| D.0.1mol/L的氯化铁溶液中:H+、Na+、Br‾、I- |