要使含有Ba2+、Al3+、Cu2+、Ag+等离子的溶液中的各离子逐一形成沉淀析出,下列所选择的试剂及加入试剂的顺序最佳的是 ( )
| A.H2SO4—HCl—NaOH—CO2 | B.HCl—H2SO4—NaOH—CO2 |
| C.NaCl—Na2SO4—NaOH—H2SO4 | D.Na2SO4—NaCl—NaOH—HCl |
下列有关金属的工业制法中,正确的是
| A.炼铜:用黄铜矿(主要成分为CuFeS2)直接电解精炼得到纯度为99.9%的铜 |
| B.制铝:工业上电解熔融氯化铝来制备铝 |
| C.制钠:电解饱和NaCl溶液 |
| D.炼铁:用CO在高温下还原铁矿石中的铁 |
X、Y、Z、W均为中学化学中常见物质或其溶液,一定条件下它们之间有如下转化关系(其它产物已略去),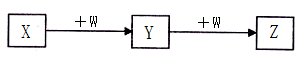
下列说法不正确的是
| A.若W是单质铁,则Z溶液可能是FeCl2溶液 |
| B.若X是碳酸钠,则W可能是盐酸 |
| C.若W是氢氧化钠,则X与Z可反应生成Y |
| D.若W为氧气,则Z与水反应(或溶于水)一定生成一种强酸 |
下列离子方程式中,正确的是
| A.Na2O2与H2O反应:Na2O2 + H2O= 2Na+ + 2OH-+ O2↑ |
| B.AlCl3溶液中滴加过量的氨水:Al3+ +4 NH3·H2O=AlO2— + 2H2O + 4NH4+ |
| C.铜与浓硝酸反应:Cu +4H+ + 2NO3- = Cu2+ + 2NO2↑ + 2H2O |
| D.向小苏打溶液中滴入醋酸:CO32-+ 2CH3COOH=CO2↑+ H2O+ 2CH3COO- |
下列各组离子在溶液中能大量共存的是
| A.Ca2+、HCO3-、Cl-、K+ | B.Al3+、AlO2-、H+、Na+ |
| C.Fe2+、NH4+、SO42-、S2- | D.Fe3+、SCN-、Na+、CO32- |
配置一定物质的量浓度的硫酸溶液是,下列操作会造成所配硫酸溶液浓度偏低的是
| A.洗涤了量取浓硫酸的量筒,并把洗涤液转移到容量瓶中 |
| B.转移溶液前,容量瓶中含有少量蒸馏水 |
| C.溶解硫酸用的烧杯、玻璃棒未洗涤 |
| D.定容时俯视容量瓶的刻度线 |