(12分)在烧杯里加入20 mL 0.1 mol/L的Ba(OH)2溶液,再滴几滴酚酞试液,然后用滴定管向烧杯中滴加等物质的量浓度的NaHSO4溶液。实验装置如下图(夹持仪器已去掉):
实验现象如下:
①灯泡逐渐变暗;
②烧杯中有白色沉淀生成,溶液红色变浅甚至消失。
请依据实验现象回答下列问题:
(1)灯泡变暗的原因是__________________________________________________。
(2)有白色沉淀生成,说明______________________________________________,
红色变浅说明________________________________________________________。
(3)当Ba2+恰好完全沉 淀时,消耗NaHSO4溶液的体积为______ mL,溶液呈______色,离子反应方程式为_________
淀时,消耗NaHSO4溶液的体积为______ mL,溶液呈______色,离子反应方程式为_________ ___________________________________________________。
___________________________________________________。
(4)若向(3)得到的 溶液中,继续滴加NaHSO4溶液到恰好变为无色,此阶段的离子反应方程式为___________________________________________________________________。
溶液中,继续滴加NaHSO4溶液到恰好变为无色,此阶段的离子反应方程式为___________________________________________________________________。
化学是一门以实验为基础的学科,化学所取得的丰硕成果,是与实验的重要作用分不开的。结合下来实验常用到的仪器回答问题:
(1)填写以下仪器的名称:B D E G 。
(2)用四氯化碳提取出溴水中Br2单质的方法叫做: ,将Br2的四氯化碳溶液和水分离开的操作叫做: ,下列是进行该操作的步骤,正确的是顺序是: 。
①将混合物倒入分液漏斗中,并放在铁架台的铁圈上静置,分层;
②从分液漏斗上口倒出上层溶液
③将分液漏斗的玻璃塞打开或使玻璃塞上的凹槽对准漏斗颈部的小孔
④分液漏斗下面导管紧贴烧杯内壁,旋开活塞,用烧杯接受溶液
⑤检查分液漏斗活塞和颈部的玻璃塞是否漏水
(3)已知Br2的沸点是58.5°C,四氯化碳沸点是78°C。将Br2的四氯化碳溶液分离开的方法是 。需要用到的玻璃仪器有(填字母) 。
(原创)重庆一中某化学兴趣小组,欲在常温常压下,用一定质量的铜镁合金与足量稀盐酸反应,利用下图装置,测定样品中铜的质量分数。
A B C
(1)实验反应原理:写出镁与稀盐酸发生反应的化学方程式________________
(2)仪器识别:写出上图中仪器①、②的名称:①_________②__________
(3)装置连接:a→___________→___________→d
(4)A中反应已经进行完毕的现象为__________________________
(5)实验中,该兴趣小组同学测得以下数据
a.反应前样品铜镁合金的质量,记为m1 g
b.反应结束后,经过处理后的残余固体的质量,记为m2 g
c.经过一系列正确的操作后,读取量筒中的水的体积,记为V mL
d.查阅资料,常温常压下,H2的密度为ρ g/L
四位同学分成甲、乙两个小组,甲组同学利用重量法为思路,请合理选择以上数据,列式求铜的质量分数:________×100%;乙组同学利用排水法测量气体体积为思路,请合理选择以上数据,列式求铜的质量分数:________×100%
(6)误差分析环节中指导教师提出,甲、乙两组同学的思路中,会有很多因素导致测得的铜的质量分数出现误差,现将可能导致误差的因素罗列如下,并回答相关问题
a.读取量筒中水的体积时,未等装置中气体恢复至室温
b.读取量筒中水的体积时,俯视量筒
c.实验开始前,没有检查装置气密性,然而装置实际是漏气的
d.B瓶中残留的空气的干扰
e.未除去样品铜镁合金表面的氧化膜便进行称量
f.未对反应中挥发出的HCl气体进行除杂处理
g.未对反应后剩余的残余物进行洗涤
h.未考虑B、C装置间连接导管中残留的水
导致铜的质量分数大于理论值的原因可能是___________________(填符号a~h)
导致铜的质量分数小于理论值的原因可能是___________________(填符号a~h)
(原创)海洋中含有丰富的宝贵资源,除了制备粗盐,还可以提取碘,冶炼金属镁等。
I.海藻中含有丰富的碘元素,碘元素以I﹣的形式存在,Cl2可以将I﹣氧化得到碘单质,实验室从海藻中提取碘单质的实验流程如下:
(1)请写出相关操作的名称:①_____________________;③_______________________
(2)如果要求有色层在上层,可以选择_______________试剂进行碘单质的萃取(填字母)
| A.醋酸 | B.苯 | C.四氯化碳 | D.汽油 |
(3)实验中的“后期处理”主要是指分液和蒸馏,蒸馏采用实验装置如下图所示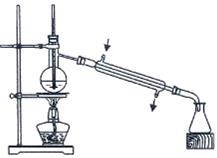
此图中的错误共有_________处(填数字)
II.海水经淡化可获得淡水和浓海水,浓海水中主要含有离子Na+、Mg2+、Cl﹣、SO42﹣。从浓海水中提取金属镁的一般工艺流程如下: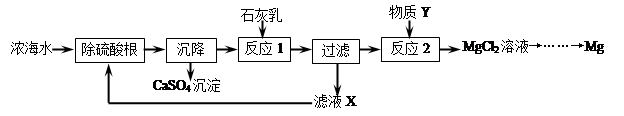
(1)补全由贝壳(主要成分为碳酸钙)生产石灰乳的相应转化中所需的条件或反应物: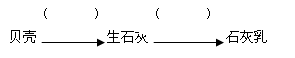
(2)写出反应2的化学方程式: 。
(3)操作流程中可循环使用的滤液X中的物质是 (填化学式)。
次硫酸氢钠甲醛(NaHSO2•HCHO•2H2O)俗称吊白块,不稳定,120℃时会分解。在印染、医药以及原子能工业中有广泛应用。以Na2SO3、SO2、HCHO和锌粉为原料制备次硫酸氢钠甲醛的实验步骤如下:
步骤1:在三颈烧瓶中加入一定量Na2SO3和水,搅拌溶解,缓慢通入SO2,至溶液pH 约为4,制得NaHSO3溶液。
步骤2:将装置A 中导气管换成橡皮塞。向烧瓶中加入稍过量的锌粉和一定量甲醛溶液,在80~90℃下,反应约3h,冷却至室温,抽滤;
步骤3:将滤液真空蒸发浓缩,冷却结晶。
(1)装置B 的烧杯中应加入的溶液是 ;冷凝管中冷却水从 (填“a”或“b”)口进水。
(2)A中多孔球泡的作用是 。
(3)冷凝管中回流的主要物质除H2O 外还有 (填化学式)。
(4)写出步骤2中发生反应的化学方程式 。
(5)步骤3中在真空容器中蒸发浓缩的原因是 。
(6)为了测定产品的纯度,准确称取2.0g样品,完全溶于水配成100mL溶液,取20.00mL所配溶液,加入过量碘完全反应后(已知I2不能氧化甲醛,杂质不反应),加入BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重得到白色固体0.466g,则所制得的产品的纯度为 。
硫代硫酸钠又名“大苏打”,溶液具有弱碱性和较强的还原性,是棉织物漂白后的脱氯剂,定量分析中的还原剂。硫代硫酸钠(Na2S2O3)可由亚硫酸钠和硫粉通过化合反应制得,装置如图所示
已知:Na2S2O3在酸性溶液中不能稳定存在。
(1)某研究小组设计了制备Na2S2O3·5H2O装置和部分操作步骤如下:
步骤1:如图连接好装置后, ,将D中导管末端浸入水中,微热烧瓶观察气泡和水柱检查装置A、C、D气密性。
步骤2:加入药品,打开K1、关闭K2,向圆底烧瓶中加入足量浓硫酸,加热。装置B中的药品可选用下列物质中的。
A.NaOH溶液 B.浓H2SO4 C.酸性KMnO4溶液 D.饱和NaHSO3溶液
步骤3:C中混合液被气流搅动,反应一段时间后,硫粉的量逐渐减少,当C中溶液的pH接近7时,打开K2,关闭K1即停止C中的反应,停止加热。“当C中溶液的pH接近7时即停止C中的反应”的原因是______________________(用离子方程式表示)。
步骤4:过滤C中的混合液,将滤液经过加热浓缩,趁热过滤,再将滤液冷却结晶、过滤、洗涤、烘干,得到产品。
(2)Na2S2O3性质的检验:向足量的新制氯水中滴加少量Na2S2O3溶液,氯水颜色变浅,检查反应后溶液中含有硫酸根,写出该反应的化学方程式_________________。
(3)常用Na2S2O3溶液测定废水中Ba2+浓度,步骤如下:取废水25.00mL,控制适当的酸度加入足量K2Cr2O7溶液,得BaCrO4沉淀;过滤、洗涤后,用适量稀盐酸溶解,此时CrO42-全部转化为Cr2O72-;再加过量KI溶液,充分反应后得混合溶液VmL,将其分成4等份,加入淀粉溶液作指示剂,用0.0010mol·L-1的Na2S2O3溶液进行滴定,相关数据记录如下表所示:
| 编号 |
1 |
2 |
3 |
4 |
| 消耗Na2S2O3标准溶液的体积/mL |
18.02 |
17.98 |
18.00 |
20.03 |
部分反应离子方程式为:
①Cr2O72-+6I-+14H+=2Cr3++3I2+7H2O;②I2+2S2O32-=2I-+S4O64-。
则判断达到滴定终点的现象是__________________。
废水中Ba2+的物质的量浓度为__________________。