(8分)0.2mol有机物与0.5molO2恰好完全燃烧后的产物为CO2和H2O(g)。产物经过浓硫酸后,浓硫酸的质量增加10.8g;再通过碱石灰剩余气体被完全吸收,碱石灰质量增加17.6g。
(1)燃烧后产物的物质的量分别为CO2________mol、H2O(g)__________mol。
(2)推断该有机物的分子式为_____________。
(3)若0.2mol该有机物恰好与9.2g金属钠完全反应,其核磁共振氢谱显示只有两种不同环境的H,试确定该有机物的结构简式为____________。
NO分子因污染空气而臭名昭著。近年来,发现少量的NO在生物体的许多组织中存在,它有扩张血管、免疫、增强记忆的功能,而成为当前生命科学研究的热点,NO亦被称为“明星分子”。请完成下列问题。
(1)NO对环境的危害在于____________(填以下项目的编号)。
| A.破坏臭氧层 | B.高温下能使一些金属被氧化 |
| C.造成酸雨 | D.与人体血红蛋白结合 |
(2)在含Cu+的酶的活化中心中,亚硝酸根离子可转化为NO,写出Cu+和亚硝酸根离子在酸性水溶液中反应的离子方程式_____________________________________________________。
(3)在常温下,把NO气体压缩到100个大气压,在一个体积固定的容器里加热到50 ℃,发现气体的压力迅速下降,压力降至略小于原压力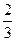 就不再改变,已知其中一种产物为N2O,写出上述变化的化学方程式_______________________________________________________。
就不再改变,已知其中一种产物为N2O,写出上述变化的化学方程式_______________________________________________________。
“神舟”5号宇宙飞船是靠长征Ⅱ(F)型运载火箭发射升空的。该火箭所用的燃料是偏二甲肼〔(CH3)2N—NH2〕,氧化剂是N2O4,产物是氮气、二氧化碳和水。
(1)火箭点火瞬间,逸出的红棕色气体是_______,产生该气体的化学反应方程式为_________。
(2)偏二甲肼在N2O4中燃烧的化学方程式为_________________________,当有1 mol偏二甲肼燃烧时,转移电子的物质的量为___________。
pH=2的某酸HnA与pH=12的某碱B(OH)m等体积混合后溶液的pH=8。
(1)写出正盐的化学式:______________________________。
(2)若该盐中只有一种离子水解,该离子水解的离子方程式为_________________________。
(3)简述该混合液呈碱性的原因。
BiCl3水解产物中有BiOCl生成。
(1)写出水解反应方程式______________________。
(2)医药上将BiOCl称为次氯酸铋,该名称____________(填“正确”“不正确”)。
(3)如何配制BiCl3溶液?
将0.02mol·L-1的HCN与0.02mol·L-1NaCN溶液等体积混合,已知该混合溶液中c(Na+)>c(CN-),用“>、<或=”填空。
(1)c(OH-)________c(H+)。
(2)c(HCN)________c(CN-)。
(3)c(HCN)+c(CN-)________0.02mol·L-1。