尿素(H2NCONH2)是一种非常重要的高氮化肥,工业上合成尿素的反应分为如下两步:
第1步:2NH3(l)+CO2(g) H2NCOONH4(氨基甲酸铵) (l) △H1=" —330.0" kJ·mol-1
H2NCOONH4(氨基甲酸铵) (l) △H1=" —330.0" kJ·mol-1
第2步:H2NCOONH4(l) H2O(l)+H2NCONH2(l) △H2="+226.3" kJ·mol-1
H2O(l)+H2NCONH2(l) △H2="+226.3" kJ·mol-1
(1)写出工业合成尿素的热化学方程式:
(2)下列措施中有利于提高尿素的产率的是___________。
| A.采用高温 | B.采用高压 | C.添加高效催化剂 | D.定时分离尿素 |
(3)某实验小组模拟工业上合成尿素的条件,在一体积为0.5 L密闭容器中投入4 mol氨和1mol二氧化碳,实验测得反应中各组分随时间的变化如下图所示: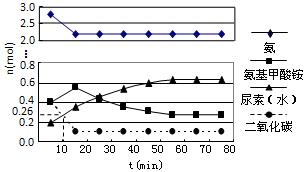
①已知总反应的快慢由慢的一步决定,则合成尿素总反应的快慢由第 步反应决定。
②反应进行到10 min时测得CO2的物质的量如上图所示,则用CO2表示的第一步反应的速率v(CO2)= 。
(4)工业上合成氨常与尿素生产联合进行以提高经济效益,合成氨的热化学方程式如下:
N2(g) + 3H2(g)  2NH3(g) △H = —92.4 kJ/mol
2NH3(g) △H = —92.4 kJ/mol
请在答题卡的坐标图中,画出反应过程中体系的能量变化图(进行必要的标注)。
(5)有一工业投产前小实验:在一定温度和压强下,将6 molH2和2 molN2在2L密闭容器中混合,当该反应达到平衡时,测得平衡混合气中NH3的体积分数约为11.1%(即1/9),此时H2的转化率是多少?(写出计算过程,计算结果保留3位有效数字。)
有A、B、C、D四种元素,A元素形成的-2价阴离子比氦的核外电子数多8个。B元素的一种氧化物为淡黄色固体,该固体遇到空气能生成A的单质。C为原子核内有12个中子的二价金属,当2.4gC与足量热水反应时,在标准状态下放出氢气2.24L。D的M层上有7个电子。
(1) A、B、C、D各是什么元素(写元素符号):
ABCD
(2)用电子式表示C与D形成化合物的过程:
。
(3)写出B、D的最高价氧化物的水化物反应的离子方程式:
。
某温度时,在2L容器中X、Y、Z三种物质随时间的变化关系曲线如图所示。
(1)由图中的数据分析,该反应的化学方程式为;
(2)反应开始至5min Z的平均反应 速率为, X的转化率为;
速率为, X的转化率为;
(3)5min后Z的生成速率比5min末Z的生成速率(大、小、相等)。
A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。
(1)A中反应的离子方程式为____________________。
(2)B中Sn极的电极反应式为____________________,
Sn极附近溶液的pH___________(填“增大”、“减小”或“不变”)。
(3)比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是____ ____________________。
____________________。
(1)下列反应中,属于放热反应的是,属于吸热反应的是。
①燃烧反应②炸药爆炸③酸碱中和反应④二氧化碳通过炽热的碳
⑤食物因氧化而腐败⑥Ba(OH)2·8H2O与NH4Cl反应⑦铁粉与稀盐酸反应
(2)写出(1)中⑥的化学方程式。
利用核磁共振技术测定有机物分子的三维结构的研究获得了2002年诺贝尔化学奖。在有机物分子中,不同氢原子的核磁共振谱中给出的峰值(信号)也不同, 根据峰值(信号)可以确定有机物分子中氢原子的种类和数目。
根据峰值(信号)可以确定有机物分子中氢原子的种类和数目。
(1)下列物质中,其核磁共振氢谱中给出的峰值(信号)只有一个的是。
| A.CH3CH3 | B.CH3COOH | C.CH3COOCH3 | D.CH3OCH3 |
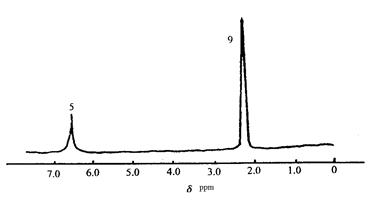
(2)化合物A和B的分子 式都是C2H4Br2, A的核磁共振氢谱图如下图所示,则A的结构简式为:,请预测B的核磁共振氢谱上有个峰(信号)。
式都是C2H4Br2, A的核磁共振氢谱图如下图所示,则A的结构简式为:,请预测B的核磁共振氢谱上有个峰(信号)。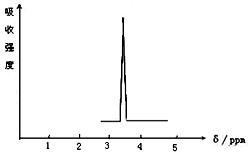
(3)化合物C的分子式是C10H14,核磁共振氢谱图如 下图所示,则C的结构简式为:。
下图所示,则C的结构简式为:。