钢铁工业在我国国民经济中处于十分重要的位置,工业上采用高炉冶炼,常用赤铁矿、焦炭、空气和熔剂(石灰石)作原料。已知赤铁矿被还原剂还原时是逐级进行的,还原时温度及CO、CO 2平衡混合气体中CO的体积分数的关系如下图:

(1)铁在元素周期表中位于 周期 族
(2)在温度低于570℃时,还原分两阶段完成,在温度高于570℃时,依次发生的还原反应有: (选用右图中的a、b、c、d填空)
(3)为减少高炉冶铁时,含CO的尾气排放,下列研究方向不可取的是 。
(a)其它条件不变,增加高炉的高度
(b)调节还原时的炉温
(c)增加原料中焦炭与赤铁矿的比例
(d)将生成的铁水及时移出
(4)已知下列反应数值:
| 反应序号 |
化学反应 |
反应热 |
| ① |
Fe 2O 3(s)+3CO(g)=2Fe(s)+3CO 2(g) |
△H 1= -26.7kJ·mol -1 |
| ② |
3Fe 2O 3(s)+CO(g)=2Fe 3O 4(s)+CO 2(g) |
△H 2= -50.8kJ·mol -1 |
| ③ |
Fe 3O 4(s)+CO(g)=3FeO(s)+CO 2(g) |
△H 3= -36.5kJ·mol -1 |
| ④ |
FeO(s)+CO(g)=Fe(s)+CO 2(g)  |
△H 4 |
反应④△H 4= kJ·mol -1。
某课外研究小组,用含有较多杂质的铜粉,通过不同的化学反应制取胆矾。其设计的实验过程为: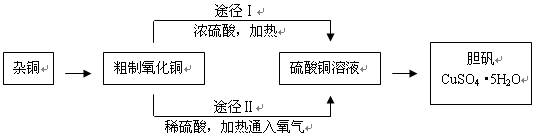
(1)铜中含有大量的有机物,可采用灼烧的方法除去有机物,灼烧是将瓷坩埚置于上(用以下所给仪器编号填入,下同),取用坩埚应使用,灼烧后的坩埚应放在上,不能直接放在桌面上。
实验所用仪器:a.蒸发皿 b.石棉网 c.泥三角 d.表面皿 e.坩埚钳 f.试管夹
(2)杂铜经灼烧后得到的产物是氧化铜及少量铜的混合物,用以制取胆矾。灼烧后含有少量铜的可能原因是()(填字母编号,有两个选项符合题意。)
a.灼烧过程中部分氧化铜被还原 b.灼烧不充分铜未被完全氧化
c.氧化铜在加热过程中分解成铜 d.该条件下铜无法被氧化
(3)由粗制氧化铜通过两种途径制取胆矾,与途径Ⅰ相比途径Ⅱ有明显的两个优点:
、
(本题12分)有机物A是一种重要化工生产的中间体,其结构简式为:C6H5-CH2CH(OH)COOH
(1)A中含有的官能团有:、(填名称)。
(2)A可能具有的化学性质有:(填序号)
①能与H2发生加成反应;②能与在烧碱溶液中发生水解反应;③能与甲酸发生酯化反应;④能金属钠发生反应,且有机物A与反应生成的氢气物质的量之比为1∶1反应;⑤能与Ag(NH3) 2OH溶液发生银镜反应。
(3)写出A分别与乙醇、乙酸发生酯化反应的方程式:
。
(4)在催化剂Pt的作用下,A与H2加成后的生成物的结构简式为。
元素在周期表中的位置,反映了元素的原子结构和元素性质。下图是元素周期表的一部分。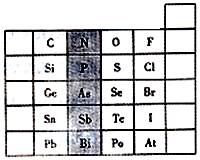
(1)阴影部分中元素N在元素周期表中的位置为第周期族,其单质分子中含有的共用电子对数目为对。
(2)根据元素周期律,请你预测H3AsO4、H3PO4、
的酸性强弱:H3AsO4H3PO4(填“>”、“<”或“=”)。
(3)在一定条件下,S、Se都能与H2反应,根据元素周期律判断,Se与H2反应比S与H2的反应。(填“更难”或“更易”)
X、Y、Z、W四种元素都是短周期元素,且原子序数W>Z>Y>X.已知:X与Y的原子的最外层电子数之和与Z原子最外层电子数相等;X的阳离子半径是自然界中离子半径最小的;W和 Y原子的最外层电子数之和是Z原子最外层电子数的2倍;W原子的最外层电子数为其电子层数的3倍.试回答:
(1)写出元素符号:X、Y、Z、W.
(2)上述元素单质中熔点最高的是.
(3)由上述四种元素组成的离子晶体在300℃完全分解为气态混合物,且混合气体的平均相对分子质量为24.该离子晶体的化学式是.
有50mL氢气和氯气的混合气体,经光照发生爆炸反应后恢复到原来的温度和压强,发现体积仍是50mL.试回答:
(1)若H2反应完全而Cl2有剩余,用实验进行验证的方法是;
(2)若H2与Cl2恰好完全反应,用实验进行验证的方法是.