红磷 P (s)和 Cl2(g)发生反应生成 PCl3(g)和 PCl5(g)。如图所示(图中的△H表示生成 l mol 产物的数据)。
根据上图回答下列问题:
(1)P和CI2反应生成 PC13的热化学方程式是______________________________;
(2)PC15分解成 PC13和 Cl2的热化学方程式是_____________________________;上述分解反应是一个可逆反应。温度 Tl时,在密闭容器中加人 0.80 mol PC15,反应达平衡时 PC15还剩 0.60 mol ,其分解率 al等于_________________;若反应温度由 Tl升高到T2,平衡时 PC15的分解率为a2,a2_________ al(填“大于”、“小于”或“等于”) ;
(3)工业上制备 PC15通常分两步进行,先将 P 和 C12反应生成中间产物 PC13,然后降温,再和Cl2反应生成 PCl5。原因是___________________________________
______________________________________________________;
(4)P 和 C12分两步反应生成 1 mol PC15的△H3==__________________,一步反应生成 1 molPC15的△H4____________△H3(填“大于”、“小于”或“等于”)。
(5)PC15与足量水充分反应,最终生成两种酸,其化学方程式是
______________________________________________________________________。
加热时,N2O5可按下列分解:N2O5 N2O3 + O2,N2O3又可按下列分解: N2O3
N2O3 + O2,N2O3又可按下列分解: N2O3 N2O + O2。今将 4 molN2O5充入一升密闭容器中,加热至 t℃时反应达到了平衡状态。平衡时,c(O2)=" 4.5" mol/L, c(N2O3)=" 1.62" mol/L,c(N2O)=mol/L,此时N2O5的分解率为。
N2O + O2。今将 4 molN2O5充入一升密闭容器中,加热至 t℃时反应达到了平衡状态。平衡时,c(O2)=" 4.5" mol/L, c(N2O3)=" 1.62" mol/L,c(N2O)=mol/L,此时N2O5的分解率为。
(1)下列四种粒子中,半径按由大到小的排列顺序是 。
①基态X的原子结构示意图:○+16
②基态Y的价电子排布式:3s23p5
③基态Z2-的电子排布图: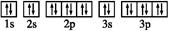
④W基态原子有2个能层,电子式:∶∶
(2)已知An+、B(n+1)+、Cn-、D(n+1)-都具有相同的电子层结构,则A、B、C、D的原子半径由大到小的顺序是 ,离子半径由大到小的顺序是 ,原子序数由大到小的顺序是 。
在恒温时,向某密闭容器中通入2mol X和1mol Y气体,发生如下反应:
2X(气)+Y(气) 2Z(气),压强一定时,测得在平衡时Z的体积分数为0.4。
2Z(气),压强一定时,测得在平衡时Z的体积分数为0.4。
(1)与上述平衡保持同温、同压,若向密闭容器中通入4mol X(气)、2mol Y(气),达到平衡,则Z的体积分数为;平衡时,气体的总物质的量是。
(2)若向密闭器中通入X(气)和Y(气)的物质的量分别记为n(X)、n(Y),保持容器容积不变,并满足平衡时Z的体积分数为0.4,则n(X)/n(Y)的取值范围为。
一定条件下,可逆反应:A2+B2 2C达到平衡。经测定,平衡时c(A2)=0.5mol/L,c(B2)=0.1mol/L,c(C)=1.6mol/L,若A2、B2和C的起始浓度分别为amol/L,bmol/L,cmol/L。
2C达到平衡。经测定,平衡时c(A2)=0.5mol/L,c(B2)=0.1mol/L,c(C)=1.6mol/L,若A2、B2和C的起始浓度分别为amol/L,bmol/L,cmol/L。
请回答:
(1)a、b应满足的关系是 (2)a的取值范围是
在2L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如图。反应在t时到达平衡,依图所示: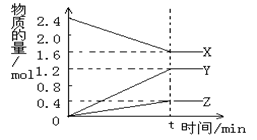
①该反应的化学方程式是 。
②反应起始至t,Y的平均反应速率是。