根据下表中烃的分子式排列规律,判断空格中烃的同分异构体数目是
| 1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
||||
| CH4 |
C2H4 |
C3H8 |
C4H8 |
|
C6H12 |
C7H16 |
C8H16
|
化学与生产和生活密切相关,下列说法正确的是
| A.聚氯乙烯塑料薄膜可用作食品保鲜膜、一次性食品袋等 |
| B.煤经过气化和液化等物理变化可转化为清洁燃料 |
| C.淀粉、油脂和蛋白质都是高分子化合物 |
| D.利用粮食酿酒经历了淀粉→葡萄糖→乙醇的化学变化过程 |
空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充放电池.图为RFC工作原理示意图,有关说法正确的是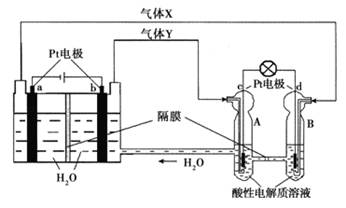
A. 当有0.1mol电子转移时,a极产生1.12L O2(标准状况下)
B. b极上发生的电极反应是:4H2O+4e﹣=2H2↑+4OH﹣
C. d极上发生的电极反应是:O2+4H++4e﹣=2H2O
D. c极上进行还原反应,B中的H+可以通过隔膜进入A
有0.1mol•L﹣1的三种溶液:①CH3COOH、②NaOH、③CH3COONa,下列说法正确的是
| A.溶液①中,c(CH3COO﹣)=c(H+) |
| B.溶液①、②等体积混合,混合液中c(CH3COO﹣)等于溶液③中的c(CH3COO﹣) |
| C.溶液①、②等体积混合,混合液中c(CH3COO﹣)+c(CH3COOH)=c(Na+) |
| D.溶液①、③等体积混合,混合液中c(Na+)>c(CH3COO﹣)>c(H+)>c(OH﹣) |
两体积相同的密闭容器中均充入1mol X和1mol Y,分别于300℃和500℃开始发生反应:X(g)+Y(g) 3Z(g).Z的含量(Z%)随时间t的变化如图所示.已知在t3时刻改变了某一实验条件.相关判断正确的是
3Z(g).Z的含量(Z%)随时间t的变化如图所示.已知在t3时刻改变了某一实验条件.相关判断正确的是
| A.曲线a是500℃时的图象 | B.t3时刻可能是降低了温度 |
| C.正反应是吸热反应 | D.t3时刻可能是增大了压强 |
对于可逆反应:A(g)+3B(g)⇌AB3(g)△H<0下列图象中正确的是
A. |
B. |
C.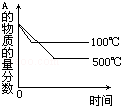 |
D.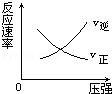 |