(13分)有一白色固体混合物,可能含有的阴、阳离子分别是
| 阳离子 |
K+ Ba2+ Ag+ Mg2+ NH Na+ |
| 阴离子 |
SO SO CO AlO |
为了鉴定其中的离子,现进行如下实验,根据实验现象,填写下列表格:
(1)取该粉末,加水后得到无色溶液,且未嗅到气味;用pH试 纸测得溶液的pH为12。
纸测得溶液的pH为12。
| 排除的离子 |
排除的依据 |
| NH Ag+、Mg2+ |
由于溶液呈碱性,且未嗅到刺激性气味,碱性溶液中无沉淀生成 |
(2)向溶液中滴加盐酸溶液,开始有沉淀生成,继续滴加,沉淀消失,同时有无色无味气体逸出。
| 肯定存在的离子 |
|
| 简述判断依据 |
|
| 排除的离子 |
|
| 简述排除的依据 |
|
(3)尚待检验的离子及其检验方法
| 尚待检验的离子 |
|
简述 检验方法 检验方法 |
|
(15分,除标明外,每空2分)已知草酸是酸性强于醋酸的二元弱酸,对应的钙盐(CaC2O4)不溶于醋酸,能溶于强酸,它还是一种还原性较强的物质。下图是利用饱和草酸溶液与KClO3粉末在60℃时反应制得ClO2,ClO2是一种黄绿色有刺激性气味的气体,熔点-59℃,沸点11-0℃。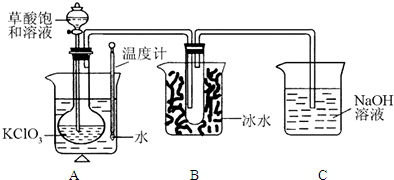
(1)该反应的反应原理如下,试配平该化学方程式KClO3+ H2C2O4=KHCO3+ClO2↑。
(2)B装置的作用是。
(3)C装置是尾气处理装置,反应一段时间后,C中含有NaOH、NaClO2、NaClO3等溶质,有同学说,C中还可能含有Na2CO3,试分析可能的原因:。
(4)某同学查资料得知“菠菜中富含可溶性草酸盐和碳酸盐”,他将菠菜研磨成汁、热水浸泡、过滤得到溶液,调节溶液呈碱性,加入足量的CaCl2溶液,产生白色沉淀,过滤、洗涤,沉淀备用,对生成的沉淀进行探究。
①提出合理假设
假设1:只存在CaCO3;
假设2:既存在CaCO3,也存在CaC2O4;
假设3: 。
②基于假设2,设计实验方案,进行实验。请在答题卷上写出实验步骤以及预期现象和结论。限选实验试剂:1 mo1·L-l H2SO4溶液、0.mo1·L-l盐酸、0.01 mo1·L-l KMnO4溶液、澄清石灰水。
| 实验步骤 |
预期现象和结论 |
| 步骤1:____ |
___________________ |
| 步骤2:____ |
___________________ |
(10分)维生素C(又名抗坏血酸,分子式为C6H8O6)具有较强的还原性,放置在空气中易被氧化,其含量可通过在弱酸性溶液中用已知浓度的I2溶液进行滴定。该反应的化学方程式如下:
C6H8O6+I2===C6H6O6+2HI
现欲测定某样品中维生素C的含量,具体的步骤及测得的数据如下:
取10 mL 6 mol·L-1CH3COOH溶液,加入100 mL蒸馏水,将溶液加热煮沸后冷却。精确称取0.2000 g样品,溶解于上述冷却的溶液中,加入1 mL指示剂,立即用浓度为0.05000 mol·L-1的I2溶液进行滴定到终点,消耗21.00 mL I2溶液。
(1)实验中的指示剂是_____________。
(2)加入的CH3COOH稀溶液要先经煮沸、冷却后才能使用。煮沸的目的是________________;冷却的目的是__________________。
(3)计算样品中维生素C的质量分数(要求列式,且式中各物理量带单位)。
某同学用0.10 mol/L的HCl溶液测定未知浓度的NaOH溶液,其实验操作如下:
| A.用碱式滴定管量取20.00mLNaOH溶液注入锥形瓶,同时滴加2-3滴酚酞试液; |
| B.用待测NaOH溶液润洗碱式滴定管; |
| C.把滴定管用蒸馏水洗净; |
| D.用标准HCl溶液润洗酸式滴定管后,将标准HCl溶液注入酸式滴定管至距离刻度“0”以上2—3cm处,再把酸式滴定管固定好,调节液面; |
E.检查滴定管是否漏水;
F.另取锥形瓶,再重复以上操作1—2 次;
G.把锥形瓶放在酸式滴定管下边,瓶下垫一张白纸,边滴边摇动锥形瓶,直到加入l滴酸液后溶液颜色突变并在半分钟内不再变色为止,记下滴定管液面所在的刻度。请回答下列问题:
(1)滴定操作的正确顺序是:(填字母)→C→→B→→→ __。
(2)G步操作中应在锥形瓶下边垫一张白纸的作用是。
(3)D步操作中液面应调节到。
(4)当观察到锥形瓶中,时,即可读数。若滴定前平视读数,滴定终点仰视读数,则由此计算得到的NaOH溶液浓度。(填“偏大”、“偏小”、“无影响”)
某实验小组用下列装置进行乙醇催化氧化的实验。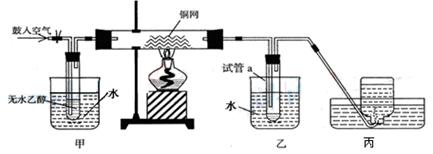
(1)请写出乙醇催化氧化的化学方程式。
在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇催化反应是反应(填“吸热”或“放热”)。
(2)甲和乙两个水浴作用不相同。
甲中盛(填“热水”或“冷水”)作用是;乙中盛(填“热水”或“冷水”)作用是。
(3)丙中集气瓶内收集到的气体的主要成分是。
(4)如何要检验试管a中收集到的反应生成物。
(1)在实验室里制取乙烯常因温度过高而使乙醇和浓H2SO4反应生成少量的SO2,有人设计如下图所示实验以确认上述混和气体中有C2H4和SO2。(乙烯的制取装置略)
①Ⅰ、Ⅱ、Ⅲ、Ⅳ装置可盛入的试剂是Ⅰ__________、Ⅱ__________、Ⅲ__________、Ⅳ__________。(将下列有关试剂的序号填入空格内)
A.品红溶液 B.NaOH溶液 C.浓H2SO4 D.KMnO4酸性溶液
② 乙醇制取乙烯的反应装置此处略去,写出该反应的化学方程式:
③ 能说明SO2气体存在的现象是_____________________________________________。
④ 使用装置Ⅲ的目的是_____________________________________________________。
⑤ 确定含有乙烯的现象是___________________________________________________。
(2)1,2-二溴乙烷可作汽油抗爆剂的添加剂,常温下是无色液体,密度2.18g/cm3,沸点131.4℃,熔点9.79℃,不溶于水、易溶于醇、醚、丙酮等有机溶剂。在实验中可以用乙烯来制备1,2-二溴乙烷。 请填写下列空白:
①写出用乙烯制备1,2-二溴乙烷的化学方程式:。
②要检验某溴乙烷中的溴元素,正确的实验方法是
A.加入氯水振荡,观察水层是否有棕红色出现
B.滴入AgNO3溶液,再加入稀HNO3,观察有无浅黄色沉淀生成
C.加入NaOH溶液共热,冷却后加入AgNO3溶液,观察有无浅黄色沉淀生成
D.加入NaOH溶液共热,然后加入稀HNO3使溶液呈酸性,再滴入AgNO3溶液,观察有无浅黄色沉淀生成