设NA为阿伏加德罗常数的值。下列说法中错误的是 ( )
| A.标准状况下,2.24L乙烷中含有0.1NA个分子 | ||
| B.0.1 mol Na与足量水反应生成H2为0.1NA |
C.46gNO2气体中氧原子总数为2NA |
D.15g甲基(—CH3)中含的电子数为9NA |
化学无处不在,下列与化学有关的说法,正确的是
| A.纤维素在人体内可水解为葡萄糖,故可作人类的营养物质 |
| B.侯氏制碱法的工艺过程中应用了物质溶解度的差异 |
| C.碘是人体必须微量元素,所以要多多吃富含高碘酸的食物 |
| D.氯化铝是一种电解质,可用于电解法制铝 |
某稀溶液中含4molKNO3和2.5molH2SO4,向其中加入1.5molFe粉,充分反应后产生的NO气体在标准状况下的体积为( )
| A.36L | B.28L | C.22.4L | D.11.2L |
某固体混合物是由Al、(NH4)2SO4、MgCl2、FeCl2、AlCl3中的两种或几种组成,现对该混合物做如下实验,所得现象和有关数据如图所示(气体体积数据已换算成标准状况下的体积):下列说法中不正确的是( )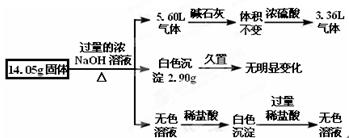
| A.该固体中一定没有FeCl2,可能含有AlCl3 |
| B.该固体中含有2.70 g Al |
| C.该固体中含有6.60 g (NH4)2SO4 |
| D.该固体中含有4.75 g MgCl2 |
X、M都是中学教材常见元素,下列对两个离子反应通式的推断中,其中正确的是( )
甲:XO3n-+X n-+H+→X单质+H2O(未配平)乙:Mm++mOH-=M(OH)m↓
①若n=1,则XO3n-中X元素为+5价,X位于周期表第ⅤA族
②若n=2,则X最高价氧化物的水化物可能与它的氢化物反应
③若m=1,则M(NO3)m溶液和氨水互滴时的现象可能不同
④若m=2,则在空气中蒸干、灼烧MSO4溶液一定能得到MSO4
⑤若m=3,则MCl3与足量氢氧化钠溶液反应一定生成M(OH)m
| A.①③ | B.④⑤ | C.①② | D.②③ |
在bLFeBr2溶液中通入amolCl2时,使溶液中50%的Br-氧化为Br2,则原FeBr2的物质的量浓度为( )
A.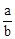 mol·L-1 mol·L-1 |
B.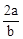 mol·L-1 mol·L-1 |
C.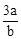 mol·L-1 mol·L-1 |
D.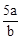 mol·L-1 mol·L-1 |