已知常温下E为无色无味的液体,F为淡黄色粉末,G为常见的无色气体(反应条件均已省略)
请回答下列问题:
(1)F的化学式为 ,H的电子式为 ,写出反应②的化学方程式 ;
(2)若A与B均为固体化合物,C是一种能使湿润的红色石蕊试纸变蓝的气体,D是一种中性干燥剂,写出反应①的化学方程式 ;
(3)若C、D均为常见气体且都能使澄清石灰水浑浊,则A是 ,B是 (写化学式);
(4)若A、C、D均含有氯元素,且A的化合价介 于C、D之间,B、C、D中均含有钾元素,写出常温时①的离子方程式: 。
于C、D之间,B、C、D中均含有钾元素,写出常温时①的离子方程式: 。
化学平衡移动原理,同样也适用于其他平衡,已知在氨水中存在下列平衡:NH3+H2O 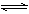 NH3·H2O
NH3·H2O 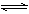 NH
NH +OH-
+OH-
(1)向氨水中加入MgCl2固体时,平衡向______移动,OH-的浓度_____,NH4+的浓度_______。
(2)向氨水中加入浓盐酸,平衡向______移动;
(3)向浓氨水中加入少量NaOH固体,平衡向_____移动,此时发生的现象是__________。
将含有Ag+、Mg2+、Al3+、Na+等离子的稀溶液,按下列实验步骤进行离子的依次分离。填写下列空白(各步可使用的试剂限于在NaOH、HCl、NaCl中选择)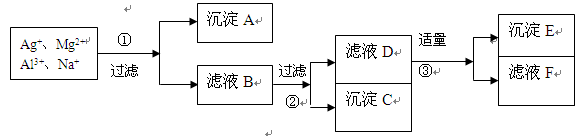
(1)沉淀A是 ___,沉淀C ___,沉淀E是;
(2)加入试剂①是 ____,②是________________,③是______________。
某种常见的白色晶体A,与盐酸反应产生无刺激性气味的气体B,将B通入澄清石灰水,石灰水变浑浊。若在A的水溶液中加氢氧化钡溶液微热,则析出白色沉淀C和无色气体D,D可以使湿润的红色石蕊试纸变蓝。加热固体A,可生成水、B和D,而且B和D的物质的量之比为1:1.根据以上事实,可以判断出A是,B是,C是。
加热固体A生成水、B和D的化学方程式是_____________,
A与盐酸反应的离子方程式___________________________________,
A与氢氧化钡溶液反应的离子方程式_______________________________________________。
如右图所示,将一瓶充满NO2气体的试管倒扣在水槽中,气体颜色由_______________逐渐变为_______色,试管内的液面会逐渐_____________,剩余气体约占试管容积的__________,用化学方程式表示这种变化__________________________;上述反应停止后向试管中缓慢通入氧气,气体颜色又由______色逐渐变为____________色,之后又变为______色,继续通入氧气,直到试管中充满液体为止,用一个化学方程式表示试管中发生的化学反应_____________________________________。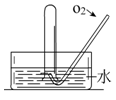
我国使用最早的合金是_____________,目前用量最大,使用最广泛的合金是___________。合金的硬度一般比它的各成分金属的硬度_________,多数合金的熔点一般比它的各成分金属的熔点___________。镁铝合金投入氢氧化钠溶液中,反应的化学方程式为__________________________,红热的铁片投入水中,表面生成一层黑色晶体,反应的化学方程式为___________________________。