已知Cr(OH)3在碱性较强的溶液中将生成[Cr(OH)4]―,铬的化合物有毒,由于+6价铬的强氧化性,其毒性是+3价铬毒性的100倍。因此,必须对含铬的废水进行处理,可采用以下还原法,在酸性介质中用FeSO4等将+6价铬还原成+3价铬。
具体流程如下:
有关离子完全沉淀的pH如下表:
| 有关离子 |
Fe2+ |
Fe3+ |
Cr3+ |
| 完全沉淀为对应氢氧化物的pH |
9.0 |
3.2 |
5.6 |
(1)写出Cr2O72―与FeSO4溶液在酸性条件下反应的离子方程式 。
(2)还原+6价铬还可选用以下的 试剂(填序号)。
A.明矾 B.铁屑 C.生石灰 D.亚硫酸氢钠
(3)在含铬废水中加入FeSO4,再调节pH,使Fe3+和Cr3+产生氢氧化物沉淀。
在操作②中调节pH应分2次进行,第1次应先调节溶液的pH范围约在 (填序号)最佳,第2次应调节溶液的pH范围约在 (填序号)最佳
A.3~4 B.6~8 C.10~11 D.12~14
用于调节溶液的最佳试剂为: (填序号);
A.Na2O2 B.Ba(OH)2 C.Ca(OH)2 D.NaOH
双酚—A的二甲基丙烯酸酯是一种能使人及动物的内分泌系统发生紊乱,导致生育及繁殖异常的环境激素,其结构简式为:
它在一定条件下水解可生成双酚—A和羧酸H两种物质。
I.(1)双酚—A的分子式为。下列有关它的叙述中正确的是。
| A.与苯酚互为同分异构体 |
| B.可以和Na2CO3溶液反应,放出CO2气体 |
| C.分子中最多有8个碳原子在同一平面上 |
| D.1mol 双酚—A与溴水反应,最多消耗Br2的物质的量为4mol |
(2)下列物质中与双酚—A互为同分异构体的是(填序号)。
II.已知与(CH3)3COH结构相似的醇不能被催化氧化为醛或酸。羧酸H可以由以下途径制得(有的反应条件没有标出):
(3)C的结构简式为。
(4)G中所含官能团为(填名称),G→H的反应类型为。
(5)E→F的化学方程式为。
水的电离平衡曲线如下图所示。
(1)若以A点表示25℃时水在电离平衡时的离子浓度, 当温度升到100℃时,水的电离平衡状态到B点,则此时水的离子积从增加到。
(2)常温下,将pH=10的Ba(OH)2溶液与pH=5的稀盐酸混合,然后保持100℃的恒温,欲使混合溶液pH=7,则Ba(OH)2与盐酸的体积比为。
(3)在某温度下,Ca(OH)2的溶解度为0.74 g,其饱和溶液密度设为1 g/mL,Ca(OH)2的离子积为。
(4))25℃时,在等体积的 ① pH=0的H2SO4溶液、②0.05mol/L的Ba(OH)2溶液,③pH=10的Na2S溶液,④pH=5的NH4NO3溶液中,发生电离的水的物质的量之比是。
(5)等体积的下列溶液中,阴离子的总物质的量最大的是_________(填序号)。
① 0.1 mol·L-1的CuSO4溶液
② 0.1 mol·L-1的Na2CO3
③ 0.1 mol·L-1的KCl
④ 0.1 mol·L-1的NaHCO3
(6)某二元酸(化学式用H2A表示)在水中的电离方程式是:H2A=H++ HA-,HA- H+ + A2- 。
H+ + A2- 。
①则Na2A溶液显________(填“酸性”“中性”或“碱性”);NaHA溶液显________(填“酸性”“中性”或“碱性”)。
②若有0.1 mol·L-1 Na2A的溶液,其中各种离子浓度由大到小的顺序是:(填序号)。
| A.c(Na+)>c(A2-)>c(OH-)>c(HA-)>c(H+) |
| B.c(Na+)>c(OH-)>c(HA-)>c(A2-)>c(H+) |
| C.c(Na+)>c(H+)>c(A2-)>c(OH-)>c(HA-) |
| D.c(A2-)>c(Na+)>c(OH-)>c(H+)>c(HA-) |
完成下列小题(共14分)
(1)右图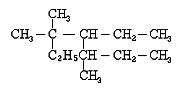 是某有机物结构简式,按系统命名法,该有机物的名称是。
是某有机物结构简式,按系统命名法,该有机物的名称是。
(2)主链含5个碳原子,有2个甲基作支链的烷烃有_______种。其中有一种同分异构体的分子,其一氯代物有4种同分异构体,写出其结构简式_____________,并对其命名____________。其中另一种同分异构体分子是由烯烃和氢气加成得到,而且该烯烃分子中的碳碳双键只有一种位置,试写出这种烯烃分子的名称______________。
(3)已知某有机物A在标况下的密度为1.34g/L,取A与氧气反应,得到等物质的量的CO2和H2O,则该有机物的分子式为______________。为测定A的结构,作核磁共振氢谱,发现只有一种吸收峰,则A可能的结构简式为____________。
向由Cu、Cu2O和CuO组成的混合物中,加入10 mL 6 mol·L-1的稀硝酸溶液,恰好使混合物完全溶解,同时收集到标准状况下NO 224 mL。请回答以下问题:
(1)写出Cu2O与稀硝酸反应的离子方程式。
(2)产物中硝酸铜的物质的量为。
(3)若原混合物中有0.01molCu,则其中Cu2O的物质的量为,CuO的物质的量为。
A、B、C为短周期元素,它们的位置关系如下图所示,已知B、C两元素原子序数之和是A元素的原子序数的4倍,则
(1)A、B、C的元素符号分别为:A_____、B_______、C____。B在周期表中的位置_______。
(2)C的离子结构示意图为_________,A的氢化物分子式为_________;
(3)B、C的最高价氧化物的水化物的酸性由强到弱的顺序为,比较B、C氢化物稳定性的强弱是。