等体积、等物质的量浓度的盐酸、氢氧化钠溶液分别放在甲、乙两烧杯中,各加等质量的铝,生成氢气的体积比为5:6,则甲、乙两烧杯中的反应情况可能分别是( )
| A.甲、乙中都是铝过量 | B.甲中铝过量、乙中碱过量 |
| C.甲中酸过量、乙中铝过量 | D.甲中酸过量、乙中碱过量 |
生活中的一些问题常涉及到化学知识,下列叙述不正确的是( )
| A.糯米中的淀粉一经发生水解反应,就酿造成酒 |
| B.福尔马林是一种良好的杀菌剂,但不可用来消毒饮用水 |
| C.棉花和人造丝的主要成分都是纤维素 |
| D.室内装饰材料中缓慢释放出的甲醛、甲苯等有机物会污染空气 |
某溶液中只可能含有下列离子中的几种(不考虑溶液中含的较少的H+和OH-)Na+、 、
、 、
、 、
、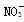 。取200 mL该溶液,分为等体积的两份做下列实验。
。取200 mL该溶液,分为等体积的两份做下列实验。
实验1:第一份加入足量的烧碱并加热,产生的气体在标准状况下为224 mL。
实验2:第二份先加入足量的盐酸,无现象,再加足量的BaCl2溶液,得固体2.33克。
下列说法正确的是( )
| A.该溶液中可能含有Na+ |
| B.该溶液中肯定含有NH4+、SO42-、CO32-、NO3- |
| C.该溶液中一定不含NO3- |
| D.该溶液中一定含Na+且c(Na+)≥0.1 mol/L |
比较MnO2和CuO对H2O2分解反应的催化能力大小的实验中,若催化剂的质量均控制在0.1 g,6%的H2O2溶液(密度按1 g·cm-3计算)均取2 mL,可选择的实验装置是( )
A. |
B. |
C. |
D. |
某同学仿照“喷泉”实验的原理,在实验室中做了一个“喷烟”实验,如图所示。他在甲、乙两个烧瓶中分别充入X、Y两种无色气体,在胶头滴管中盛有含酚酞的NaOH溶液,实验时将胶头滴管内的液体挤入甲烧瓶内,然后打开止水夹,便可看到甲烧瓶中的导管口喷出白色的烟,同时甲烧瓶中的溶液颜色逐渐变浅。若已知X、Y是HCl、NH3、Cl2、O2、CH4、SO2、NO七种气体中的两种,则下列判断中,正确的是( )
| A.X是NH3,Y是HCl | B.X是Cl2,Y是CH4 |
| C.X是SO2,Y是O2 | D.X是NO,Y是O2 |
下列实验不能达到预期目的的是( )
| 序号 |
实验内容 |
实验目的 |
| A |
Cl2、Br2分别与H2反应 |
比较氯、溴的非金属性强弱 |
| B |
Cl2、S分别与Fe反应 |
比较Cl2、S的氧化性强弱 |
| C |
测定相同浓度的Na2CO3、Na2SO4两溶液的pH |
比较碳酸、硫酸的稳定性强弱 |
| D |
用同一电路测定等浓度的盐酸、醋酸两溶液的导电性 |
比较盐酸、醋酸的酸性强弱 |