现有A、B、C、D、E五种可溶强电解质,它们在水中可电离产生下列离子(各种离子不重复)。
| 阳离子 |
H+、Na+、A13+、Ag+、Ba2+ |
| 阴离子 |
OH-、Cl-、NO3-、CO32-、SO42- |
已知:
① A、B两溶液呈碱性,C、D、E溶液呈酸性。
常温下,0.1mol/L A溶液的pH小于13,
0.1mol/L C溶液的pH小于1。
②A溶液与E溶液反应既有气体又有 沉淀产生;
沉淀产生;
A溶液与C溶液反应只有气体产生(沉淀包括微溶物,下同)。
③D溶液与另外四种溶液反应都能产生沉淀。
试回答下列问题:
(1)写出D的化学式: 。
(2)将E溶液加热蒸干并灼烧所得产物的名称为: ;
(3)写出A、E溶液反应的离子方程式: ;
(4)写出B溶液与C溶液恰好完全反应至溶液呈中性的离子方程式:
有A、B、C三种烃的衍生物,相互转化关系如下:
其中B可发生银镜反应,C跟石灰石反应产生能使澄清石灰水变浑浊的气体。A、B、C的结构简式和名称依次是_______________________________、_____________________________、_______________________________。
写出下列反应的化学方程式 A→B_______________________________________
B→C________________________________________
B→A___________________________________________
化学式为C3H8O的化合物A 具有如下性质:
① A + Na →慢慢产生气泡
② A + CH3COOH(加热条件下)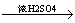 有香味的物质
有香味的物质写出A的结构简式
A在浓硫酸作用下发生消去反应生成的有机产物的结构简式为
化合物A和CH3COOH反应生成有香味的产物的结构简式为
(8分)写出下列各种烃的结构简式 2,3,3-三甲基戊烷 ___________________________;
2,3-二甲基-4-乙基己烷______________________;
间二甲苯______________________;
2-甲基-2-丁烯______________________
观察下列A、B、C、D、E五种粒子(原子或离子)的结构示意图,回答有关问题:
属于离子结构示意图的是 、 (填写微粒符号)。
五种粒子中,性质最稳定的原子是 (用微粒符号填写,在本小题中下同),最容易失去电子的原子是,最容易得到电子的原子是。
A、E两种元素形成的化合物在水溶液中的电离方程式是 。
在核电荷数为1-18的元素中,写出两种与B核外电子层排布相同的离子,其离子的符号为 、 (A-E中已出现的元素除外)。
在一定条件下,D可以和氮气(N2)化合成一种白色物质,该物质的化学式是 。
现有X、Y、Z、W四种短周期元素原子序数依次增大,其原子半径及主要化合价如下表所示。又知X与Y、Z与W分别位于同一周期,Y、W处于同一主族。
| 元素 |
X |
Y |
Z |
W |
| 原子半径/nm |
0.077 |
0.074 |
0.186 |
0.102 |
| 主要化合价 |
-4,+4 |
-2 |
+1 |
-2,+6 |
请回答: X位于元素周期表的 ,画出Z原子结构示意图 ,
Z2W是离子晶体,写出其电子式 。X单质能与某酸(H2WY4)的浓溶液发生反应,产物有XY2、WY2和水,
其反应的化学方程式为;Z2Y2可与XY2发生反应可给潜水艇供氧,其反应的化学方程式为;
若反应中转移电子数为3.01×1023,则所得气体产物的体积是(标准状况)。Y、Z、W三种元素可组成质量比为5.75 : 8 : 4的某种化合物。实验室检验该化合物中所含阴离子的操作方法及有关实验现象是:取少量含该阴离子的溶液,,则证明原溶液中含有该阴离子。