下列叙述错误的是( )
| A.带相反电荷离子之间的相互吸引称为离子键 |
| B.金属元素和非金属元素化合时不一定形成离子键 |
| C.原子最外层只有一个电子的主族元素,它与卤素结合时所形成的化学键不一定是离子键 |
| D.非金属原子之间不可能形成离子键,所以非金属原子形成的化合物中不可能含有离子键 |
下列装置或操作能达到实验目的的是
| A.图1所示装置可检查装置气密性 |
| B.图2所示装置可从碘的CCl4溶液中分离出碘 |
| C.图3所示装置可除去甲烷中乙烯 |
| D.图4所示装置可分离甲苯与乙醇 |
由2-氯丙烷制取少量的1,2-丙二醇时,需要经过的各反应分别为
| A.加成反应,消去反应,取代反应 | B.消去反应,加成反应,取代反应 |
| C.取代反应,消去反应,加成反应 | D.取代反应,加成反应,消去反应 |
下列物质既能发生消去反应,又能发生水解反应的是
| A.一氯甲烷 | B.2-甲基-1-溴丙烷 |
| C.2,2-二甲基-1-氯丙烷 | D.2,2,4,4-四甲基-3-氯戊烷 |
下列有关化学用语表示正确的是
| A.乙醇的结构简式C2H6O |
B.氨基的电子式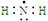 |
C.镁离子的结构示意图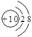 |
D.中子数为79、质子数为55 的铯(Cs)原子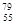 Cs Cs |
2013年4月24日,东航首次成功进行了由地沟油生产的生物航空燃油的验证飞行。能区别地沟油(加工过的餐饮废弃油)与矿物油(汽油、煤油、柴油等)的方法是
| A.点燃,能燃烧的是矿物油 |
| B.测定沸点,有固定沸点的是矿物油 |
| C.加入水中,浮在水面上的是地沟油 |
| D.加入足量氢氧化钠溶液共热,不分层的是地沟油 |