下列实验操作中错误的是( )
| A.分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 |
| B.蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 |
| C.蒸发结晶时应将溶液蒸干 |
| D.称量时,称量物放在称量纸上,置于托盘天平的左盘,砝码放在托盘天平的右盘中 |
2SO2(g) + O2(g)  2SO3(g)是工业制硫酸的主要反应之一。一定温度下,在甲、乙、丙三个容积均为2 L的恒容密闭容器中投入SO2(g)和O2(g),其起始物质的量及SO2的平衡转化率如下表所示。
2SO3(g)是工业制硫酸的主要反应之一。一定温度下,在甲、乙、丙三个容积均为2 L的恒容密闭容器中投入SO2(g)和O2(g),其起始物质的量及SO2的平衡转化率如下表所示。
| 甲 |
乙 |
丙 |
||
| 起始物质的量 |
n(SO2) / mol |
0.4 |
0.8 |
0.8 |
| n(O2) / mol |
0.24 |
0.24 |
0.48 |
|
| SO2的平衡转化率 / % |
80 |
α1 |
α2 |
下列判断中,正确的是()
A.甲中反应的平衡常数小于乙
B.该温度下,平衡常数值为400
C.平衡时,丙中c(SO3)是甲中的2倍
D.平衡时,甲中O2的转化率大于乙中O2的转化率
下列依据热化学方程式得出的结论正确的是()
| A.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-57.3 kJ·mol-1,则含40.0 g NaOH的稀溶液与稀醋酸完全中和,放出小于57.3 kJ的热量 |
| B.已知2H2(g)+O2(g)=2H2O(g)△H=-483.6 kJ·mol--1,则氢气的燃烧热为241.8 kJ·mol-1 |
| C.已知2C(s)+2O2(g)=2CO2(g)△H=a、2C(s)+O2(g)=2CO(g)△H=b,则a>b |
| D.已知P (白磷,s)=P (红磷,s)△H<0,则白磷比红磷稳定 |
有机物M的结构简式如图所示。下列说法中正确的是()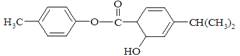
| A.分子式为C17H18O3 |
| B.M中所有碳原子均可能在同一平面 |
| C.M可以发生加成、取代、消去等反应 |
| D.1mol M常温下最多可以与3 mol NaOH反应 |
有关下列图像说法正确的是()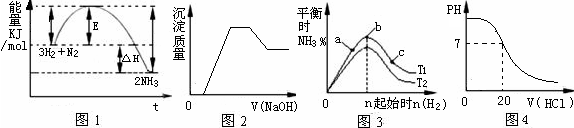
| A.由图1可知合成氨反应为自发反应,加入适当的催化剂,E和△H都减小 |
| B.图2表示向含有H+、Mg2+、Al3+、NH4+中加入NaOH溶液与产生沉淀质量的变化关系 |
| C.图3表示合成氨反应在其他条件不变的情况下,改变起始物n(H2)对此反应平衡的影响。可知反应物N2的转化率最高的是b点;T1>T2,K2> K1(T1和T2表示温度,K1、K2表示对应温度下平衡常数) |
| D.图4表示25℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1氨水的pH随加入盐酸体积的变化 |
下列实验操作与预期实验目的或所得实验结论一致的是()
| 选项 |
实验操作 |
实验目的或结论 |
| A |
向AlCl3溶液中加入过量的氨水,过滤,洗涤,干燥,加热灼烧 |
制取Al(OH)3 |
| B |
将浓硫酸与碳混合加热,生成的气体通入足量的澄清石灰水 |
检验气体产物中的CO2 |
| C |
NaHCO3溶液与NaAlO2溶液混合产生白色沉淀 |
酸性:HCO3- > Al(OH)3 |
| D |
将SO2通入品红溶液中,品红溶液褪色,加热褪色后的品红溶液,溶液恢复红色 |
验证亚硫酸的不稳定性 |