经测定一容器中只有气体,且只含C和H两种元素,通常情况下这瓶气体不可能是()
| A.一种化合物 | B.一种单质和一种化合物的混合物 |
| C.两种化合物 | D.两种单质 |
下列各式中,属于正确的电离方程式的是()
A.HCO3- + H2O H2CO3 + OH- H2CO3 + OH- |
B.HCO3- +OH- ="=" H2O + CO32- |
| C.NH3+ H+ ="==" NH4+ | D.NH3·H2O  NH4+ + OH- NH4+ + OH- |
设C(S)+CO2(g)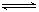 2CO(g) △H>0,反应速率为u1,N2(g)+3H2(g)
2CO(g) △H>0,反应速率为u1,N2(g)+3H2(g)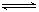 2NH3(g) △H<0反应速率为u2,对于上述反应,当温度升高时,u1和u2的变化情况为()
2NH3(g) △H<0反应速率为u2,对于上述反应,当温度升高时,u1和u2的变化情况为()
| A.同时增大 | B.同时减小 | C.增大,减小 | D.减小,增大 |
环丙烷的结构简式可表示为△,而环已烷因碳原子在空间排列方式不同,有两种空间异构体结构:船式和椅式(如图),当环已烷的不同碳原子上连有两个重氢(D)原子时,包括重氢在六个碳环上位置不同与空间异构在内的异构体共有(不考虑顺反异构)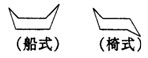
A.6种
B.12种
C.16种
D.10种
下图是198 K时N2与H2反应过程中能量变化的曲线图。下列叙述正确的是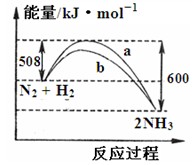
A.该反应的热化学方程式为:N2 + 3H2 2NH3△H =-92 kJ·mol-1 2NH3△H =-92 kJ·mol-1 |
| B.向一密闭容器中加入1 molN2和3 molH2充分反应后,放出92 kJ热量 |
| C.b曲线可能是加入催化剂时的能量变化曲线 |
| D.加入正催化剂可增大正反应速率,降低逆反应速率 |
已知化学反应:①C(s)+1/2O2(g) = CO(g)△H1<0
②CO(g) +1/2O2(g) = CO2(g)△H2<0
③C(s)+O2(g) = CO2(g)△H3<0;
相同条件下,下列说法正确的是
| A.56 g CO和32 g O2所具有的总能量大于88 g CO2所具有的总能量 |
| B.反应②反应物的键能之和大于产物键能之和 |
| C.△H1+△H2>△H3 |
| D.△H3 >△H1 ,故CO2比CO稳定 |