下列叙述不正确的是:
| A.液氯泄漏事故时,附近人员应迅速远离液氯泄漏地点,并逆风往安全区域疏散 |
| B.水的沸点比硫化氢高,主要原因是水分子间能形成氢键 |
| C.反应AgCl+NaBr=AgBr+NaCl能在水溶液中进行,是因为AgBr比AgCl更难溶于水 |
| D.常温下浓硫酸可贮存于铁制或铝制容器中,说明常温下铁和铝与浓硫酸不反应 |
在实验室里,储存在棕色细口瓶中的试剂是
| A.碘单质 | B.浓硝酸 | C.浓盐酸 | D.浓硫酸 |
化学与环境、材料、信息、能源关系密切,下列说法正确的是
| A.绿色化学的核心是应用化学原理对环境污染进行治理 |
| B.海水中存在大量镁单质 |
| C.大力推广燃料“脱硫、脱硝”技术,可减少硫氧化物和氮氧化物对空气的污染 |
| D.计算机芯片的材料是二氧化硅 |
相同温度下,体积均为0.25 L的两个恒容密闭容器中发生可逆反应:
N2(g)+3H2(g)  2NH3(g) ΔH =-92.6 kJ·mol-1。
2NH3(g) ΔH =-92.6 kJ·mol-1。
实验测得起始、平衡时的有关数据如下表所示,下列叙述错误的是
| 容器 编号 |
起始时各物质的物质的量/mol |
达到平衡时 体系能量的变化 |
||
| N2 |
H2 |
NH3 |
||
| ① |
1 |
3 |
0 |
放出热量:23.15 kJ |
| ② |
0.9 |
2.7 |
0.2 |
放出热量:Q kJ |
A.容器①、②中反应的平衡常数相等
B.平衡时,两个容器中NH3的体积分数均为1/7
C.容器②中达到平衡时放出的热量Q=23.15 kJ
D.若其他条件不变,把容器①的体积改为0.5 L,则平衡时放出的热量小于23.15 kJ
已知25 ℃时有关弱酸的电离平衡常数如下表:
| 弱酸化学式 |
HF |
HClO |
H2CO3 |
| 电离平衡常数 |
6.8×10-4 |
4.7×10-8 |
K1=4.3×10-7 K2=5.6×10-11 |
下列推断正确的是
A.常温下,同物质的量浓度NaClO与NaHCO3溶液,前者的pH较小
B.若某溶液中c(F—)=c(ClO—),往该溶液中滴入HCl,F-比ClO-更易结合H+
C.往饱和Na2CO3溶液中逐滴加入稀盐酸至过量,所得溶液中c(HCO3—)先增大后减小
D.同温下,等体积、等pH的HF和HClO分别与NaOH完全反应,消耗等量的NaOH
某一容器中发生如下反应:2NO(g)+O2(g)  2NO2(g); ΔH =" Q" kJ·mol-1,在其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下随温度变化的关系如图所示。下列判断正确的是
2NO2(g); ΔH =" Q" kJ·mol-1,在其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下随温度变化的关系如图所示。下列判断正确的是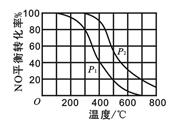
| A.p2 > p1且Q <0 |
| B.p2 > p1且Q >0 |
| C.p2 < p1且Q <0 |
| D.p2 < p1且Q >0 |