铁及其化合物之间的相互转化可用下式表示:
回答下列有关问题:
(1)Fe与过量稀硫酸反应可以制取FeSO4。若用反应所得的酸性溶液,实现上述①的转化,要求产物纯净,可选用的试剂是________(选填序号)。
a.Cl2 b.Fe c.HNO3  d.H2O2
d.H2O2
(2)上述转化得到的硫酸铁可用于电化浸出黄铜矿精矿工艺。精矿在阳极浸出的反应比较复杂,其中有一主要反应CuFeS2+4Fe3+=Cu2++5 Fe2++2S(CuFeS2中S为—2价),下列说法正确的是________(选填序号)。
Fe2++2S(CuFeS2中S为—2价),下列说法正确的是________(选填序号)。
a.从物质分类的角度看,黄铜矿属于合金
b.反应中,所有铁元素均被还原
c.反应中,CuFeS2既作氧化剂又作还原剂
d.当转移1 mol电子时,46 g CuFeS2参加反应
(3)下述反应中,若FeSO4和O2的系数比为2︰1,试配平下列方程式:
FeSO4 + K2O2→ K2FeO4 + K2O + K2SO4 + O2↑
(1)5.3gNa2CO3的物质的量是,约含有Na+个。
(2)同温同压下的氮气和氢气,若体积相同时,两种气体的质量比,其密度比为;若质量相等时,两种气体的体积比为。
(3)相同物质的量浓度、相同体积的NaCl、MgCl2、AlCl3溶液,分别与足量的AgNO3溶液反应,生成AgCl沉淀的质量之比为________。
(4)相同物质的量浓度的NaCl、MgCl2、AlCl3溶液,分别与足量的AgNO3溶液反应,当生成的AgCl质量相同时,消耗的三种溶液的体积比为________。
(5)相同浓度的NaCl、MgCl2、AlCl3溶液,分别与AgNO3溶液反应,当生成的AgCl沉淀的质量之比为3∶2∶1时,三种溶液的体积比为________。
T℃时,有甲、乙两个密闭容器,甲容器的体积为1 L,乙容器的体积为2 L,分别向甲、乙两容器中加入6 mol A和3 mol B,发生反应如下:3A(g)+bB(g) 3C(g)+2D(g) ΔH<0; 4 min时甲容器内的反应恰好达到平衡,A的浓度为2.4 mol/L,B的浓度为1.8 mol/L; t min时乙容器内的反应达平衡,根据题给信息回答下列问题:
3C(g)+2D(g) ΔH<0; 4 min时甲容器内的反应恰好达到平衡,A的浓度为2.4 mol/L,B的浓度为1.8 mol/L; t min时乙容器内的反应达平衡,根据题给信息回答下列问题:
(1)甲容器中反应的平均速率v(B)=________,化学方程式中计量数b=________.
(2)乙容器中反应达到平衡时所需时间t________4 min(填“大于”、“小于”或“等于”).
(3)若要使甲、乙容器中B的平衡浓度相等,可以采取的措施是________.
A.保持温度不变,增大甲容器的体积至2 L
B.保持容器体积不变,使甲容器升高温度
C.保持容器压强和温度都不变,向甲中加入一定量的A气体
D.保持容器压强和温度都不变,向甲中加入一定量的B气体
(4)写出平衡常数表达式K=_____________,并计算在T℃时的化学平衡常数K=_________.
已知下列热化学方程式:①2H2(g)+O2(g)=2H2O(l)△H=-570kJ/mol ,
②H2(g)+1/2O2(g)=H2O(g)△H=-241.8kJ/mol ,
③C(g)+1/2O2(g)="CO" (g) △H=" —110.5KJ/moL" ,
④C(s)+O2(g)=CO2(g) △H=—393.5KJ/moL。回答下列各问:
(1)上述反应中属于放热反应的是
(2)C的燃烧热为
(3)燃烧10gH2生成液态水,放出的热量为。
(4)CO的燃烧热为,表示CO燃烧热的热化学方程式为
(1)在一个容积为3L的密闭容器内进行如下反应:N2(气)+3H2(气)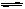 2NH3
2NH3
(气)。反应开始时,n(N2)=1.5mol,n(H2)= 4.4mol,2min后达到平衡状态,n(H2)=3.5mol。
用NH3的浓度变化来表示该反应的反应速率为___________________,2min末N2的浓度
________________,平衡时N2的转化率为______________________。
(2)在密闭容器中,对于反应:N2(g)+ 3H2(g)  2NH3(g),在反应起始时N2和H2分别
2NH3(g),在反应起始时N2和H2分别
为5mol和15mol,当达到平衡时,N2的转化率为20%。若以NH3为起始反应物,反应条
件与上述反应相同时,欲使其达到平衡时各成分的百分含量与前者相同,则NH3的起始物
质的量为,NH3的转化率。
反应A(g)+B(g)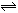 C(g)+D(g)过程中的能量变化如图所示,回答问题。
C(g)+D(g)过程中的能量变化如图所示,回答问题。
(1)该反应是反应(填“吸热”或“放热”);
(2)当反应达到平衡时,升高温度,A的转化率(填“增大”“减小”“不变”)。
(3)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1,
E2_____(填“增大”“减小”“不变”)。