在浓盐酸中H3AsO3与SnCl2反应的离子方程式为: 3SnCl2+12Cl-+2H3AsO3+6H+===2As+3SnCl62 -+6M,关于该反应的说法中正确的组合是( )
-+6M,关于该反应的说法中正确的组合是( )
①氧化剂是H3AsO3;②还原性:Cl->As;③每生成1 mol As,反应中转移电子的物质的量为3 mol;④M为OH-;⑤SnCl62-是氧化产物。
| A.①③⑤ | B.①②④⑤ | C.①②③④ | D.只有①③ |
下列微粒结构示意图中,不正确的是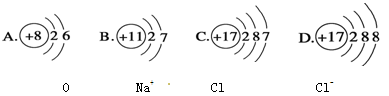
J、Q、M、R、T是原子序数依次增大的短周期主族元素,J、Q、R在周期表中的相对位置如下表。已知J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含量最多的金属元素。下列说法正确的是
| J |
Q |
|
| R |
A. J和氢元素形成的化合物分子中只含极性共价键
B. R、Q两元素形成的氢化物中,R的氢化物沸点更高
C. J、M、R、T元素最高价氧化物对应的水化物中酸性最强的是H2RO4
D. M单质能与氢氧化钠溶液反应,其中水和氢氧化钠都是氧化剂
已知氧化性:HClO>Cl2>Fe3+>SO42-;常温下,电离常数:K(H2CO3)>K(HClO)>K(HCO3-)>KAl(OH)3;则下列相关离子方程式正确的是
| A.0.5mol/L的NaHSO3溶液与1.0mol/L的NaClO溶液等体积混合:HSO3-+ClO-=SO42-+Cl-+H+ |
| B.小苏打溶液与偏铝酸钠溶液混合:HCO3-+AlO2-+H2O=Al(OH)3↓+CO32- |
| C.“84”消毒液(主要成分为NaClO)露置在空气中变质:2ClO-+CO2+H2O=CO32-+2HClO |
| D.在“84”消毒液中滴加FeSO4溶液:2Fe2++ClO-+H2O=2Fe3++Cl-+2OH- |
某有机物的结构简式如下图所示,则下列有关说法正确的是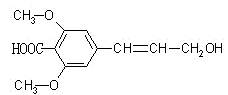
| A.该有机物可以发生氧化、加成、加聚、取代等反应 |
| B.该有机物能与NaOH溶液反应,则1mol该有机物能消耗2molNaOH |
| C.该有机物的分子式为C12H14O5,且与C11H12O5 一定互为同系物 |
| D.该有机物分子中所有碳原子不可能都在同一平面上 |
已知H2A为弱酸,下列说法错误的是
A.0.1mol/L的Na2A溶液中:c(A2-)+c(HA-)+ c(H2A)= 0.1mol/L
B.常温下,将pH=3的H2A溶液稀释到原来的100倍,则稀释后溶液的pH<5
C.常温下,将pH=3的H2A溶液与pH=11的NaOH溶液等体积混合,反应混合液呈酸性
D.常温下,若1mol/L的NaHA溶液的pH=9,则溶液中:c(Na+)-c(HA-)-c(A2-)=10-5-10-9