在生活中根据不同的分类标准可以将分散系分为各种类型,例如根据分散质 不同可将分散系分为溶液、胶体和浊液,其中分散质微粒的直径在 之间的分散系叫做胶体,胶体有很强的吸附能力,在日常生活中通常作为 剂。
2010年美、日三位科学家因钯(Pd)催化的交叉偶联反应获诺贝尔化学奖。一种钯催化的交叉偶联反应如下:
( 、
、 为烃基或其他基团)
为烃基或其他基团)
应用上述反应原理合成防晒霜主要成分K的路线如下图所示(部分反应试剂和条件未注明):
已知:①B能发生银镜反应,1 mol B最多与2 mol H2反应。
②C8H17OH分子中只有一个支链,且为乙基,其连续氧化的产物能与NaHCO3反应生成CO2,其消去产物的分子中只有一个碳原子上没有氢。
③G不能与NaOH溶液反应。
④核磁共振图谱显示J分子有3种不同的氢原子。
请回答:
(1)B中含有的官能团的名称____________。
(2)B→D的反应类型___________。
(3)D→E的化学方程式___________。
(4)有机物的结构简式:G___________;K___________。
(5)符合下列条件的同分异构体有(包括顺反异构)__________种:其中一种的结构简式是___________。
a. 与D互为同系物 b. 相对分子质量是86
(6)分离提纯中间产物E的操作:先用碱除去D和H2SO4,再用水洗涤,弃去水层,最终通过___________操作除去C8H17OH,精制得E。
迷迭香酸是存在于许多植物中的一种多酚,具有抗氧化、延缓衰老、减肥降脂等功效,其结构如下图所示。
某同学设计了迷迭香酸的合成线路:
已知:①
 、
、 表示烃基或氢原子;
表示烃基或氢原子;
②苯环上的羟基很难直接与羧酸发生酯化反应。
(1)迷迭香酸分子中所含官能团的名称是羟基、碳碳双键、___________和___________。
(2)A的结构简式为___________。
(3)C的结构简式为___________。
(4)D、E反应的化学方程式为______________________。
(5)与E互为同分异构体且同时满足下列条件的有机物有____种,写出其中任意两种同分异构体的结构简式:___________、__________。
①苯环上共有四个取代基,且苯环上只有一种化学环境的氢原子;
②1mol该同分异构体分别与NaHCO3、NaOH反应时,最多消耗NaHCO3、NaOH的物质的量分别是1mol、4mol。
化合物A经李比希法测得其中含C 72.0%、H 6.67%,其余为氧,质谱法分析得知A的相对分子质量为150。现代仪器分析有机化合物的分子结构有以下两种方法。
方法一:核磁共振仪测出A的核磁共振氢谱有5个峰,其面积之比为1:2:2:2:3。
方法二:红外光谱仪测得A分子的红外光谱下图所示: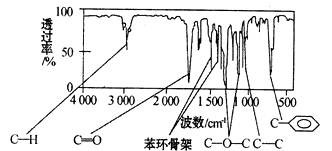
(1)A的分子式为________________。
(2)已知:A分子中只含一个苯环,且苯环上只有一个取代基,A可以水解,写出符合上述条件的A的结构简式________________(只写一种)。
(3)此A在无机酸作用下水解的化学方程式为________________。
以五倍子为原料可制得A,A结构简式为下图所示,回答下列问题:
(1)A的分子式为_______________。
(2)有机化合物B在硫酸催化条件下加热发生酯化可得到A。写出B的结构简式为____________。
(3)写出A与过量NaOH溶液反应的化学方程式_____________________。
提纯下列物质(括号内为杂质),填写所选用的除杂试剂和除杂方法
| 括号内为杂质 |
除杂试剂 |
操作 |
|
| 1 |
乙烷(乙烯) |
||
| 2 |
乙酸乙酯(乙酸) |
||
| 3 |
苯(苯酚) |
||
| 4 |
乙醇(水) |