"在学校的元旦联欢会上,某同学表演了'水能生火'的魔术.他向包有过氧化钠(
)粉末的脱脂棉上滴水,脱脂棉燃烧起来."小颖看到这段话后非常感兴趣,她和同学们一起对该问题进行了一系列的探究.
[提出问题]过氧化钠与水反应生成了什么物质?为什么脱脂棉会燃烧?
[猜 想]①可能有一种气体和另一种物质生成②反应过程中可能有能量变化
[设计装置]如图所示
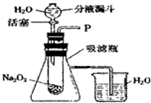
[实验探究]
实验一:探究反应后生成的气体是什么?
(1)打开右图装置中分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃.说明生成的气体是
(2)实验中,还观察到伸入烧杯中的导管口有气泡冒出,请解释产生该现象的原因:
(1)小明猜想另一种物质是
,小军认为不可能.为了证实小军的看法,请你设计一个证明
不存在的实验:
| 实验步骤 |
实验现象 |
实验结论 |
| 生成物中没有
|
(2)小军取反应后所得的溶液于试管中,滴入无色酚酞试液,发现试管中的溶液变成红色,说明反应后所得的溶液呈
碱式碳酸铜[化学式为Cu2(OH)2CO3,相对分子质量为222]加热完全分解后得到的黑色固体是什么呢?甲、乙、丙三位同学想通过实验探究,来确定该黑色固体的组成。
(1)提出问题:黑色固体是什么?
(2)猜想与假设: 黑色固体可能是:①;②可能是炭粉;③可能是炭粉和氧化铜的混合物。请你补充猜想①。作出这些猜想的依据是。
(3)实验方案: 他们称取了2.22g碱式碳酸铜在试管中高温加热使之完全分解,冷却至室温,称得黑色固体产物的质量为1.6g。
(4)实验反思:① 甲同学经过思考后,认为可以排除猜想③,理由是(用化学方程式表示)。
② 乙同学根据质量守恒定律:化学反应前后,元素的种类和质量都不变。通过对得到的数据进行计算,排除了猜想②,他的理由是(通过计算式说明)。
(5)实验结论:结合甲、乙同学的探究和查阅资料,丙同学确认只有猜想①成立。
(6)实验拓展:丙同学想进一步探究该黑色固体的化学性质。他发现实验室有一瓶无色溶液,其标签严重破损(如图),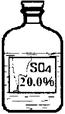
老师告诉他该瓶试剂是硫酸、硫酸钠或硫酸镁溶液中的一种。他通过查阅资料得知常温下这三种物质的溶解度如下表:
| 物 质 |
H2SO4 |
Na2SO4 |
MgSO4 |
| 常温下的溶解度∕g |
与水以任意比互溶 |
18.0 |
39.0 |
丙同学根据以上信息,分析此溶液一定不是溶液。为确定其成分,他取了少量黑色固体放入试管中,然后向其中滴加了一定量的该无色溶液后,发现黑色固体全部消失,溶液由无色变为蓝色。他确定该溶液为。其反应的化学方程式为。
(共12分)为确定木炭还原氧化铜后的固体成份,请你与兴趣小组的同学完成以下探究。
【对固体猜想】
猜想I:全部是金属铜;猜想Ⅱ:除铜外,还含有氧化铜;
猜想Ⅲ:除铜外,还含有木炭;猜想Ⅳ:除铜外,还含有氧化铜、。
【进行实验】实验流程见下图: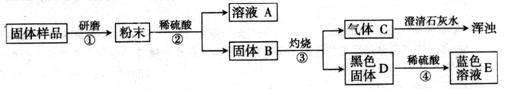
【问题与讨论】
(1)步骤②包括溶解、两步操作,它们共同用到的玻璃仪器是烧杯、。
(2)C的化学式为,D的化学式为,由此推出固体B中含有
(写化学式),步骤④发生反应的化学方程式为。
(3)结合(2)的结论推断:如果溶液A显蓝色,则溶液A的溶质的化学式为,说明样品中含有,则证明猜想成立;如果溶液A无色,则证明猜想成立。
一瓶无色液体A,含有NaCl、NaOH和Na2CO3中的两种;一包白色粉末B,含有CaO、Ca(OH)2和CaCO3中的两种。化学小组的同学为了探究A和B的成分,设计了如下图所示的实验方案,请根据图示过程回答问题。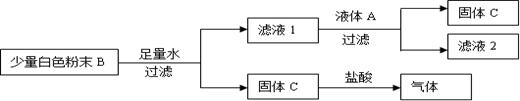
(1)固体C难溶于水,是一种常见的补钙产品,则固体C是,与盐酸反应的化学方程式为。
(2)液体A中一定含有的一种溶质为,白色粉末B中一定含有的一种物质为。试写出滤液1与液体A之间发生反应的化学方程式为。
(3)小组同学们分析发现:假设溶液A滴加适量,若滤液2中只含有一种溶质,则原无色溶液A中含有的另外一种溶质是;若滤液2中含有两种溶质,则原无色溶液A中含有的另外一种溶质是。
现欲探究一固体混合物A的成分,已知其中可能含有Mg(OH)2、FeCl3、NH4Cl、 (NH4)2SO4四种物质中的两种或多种。按图所示进行实验,出现的现象如图所示(设过程中所有可能发生的反应均恰好完全反应)。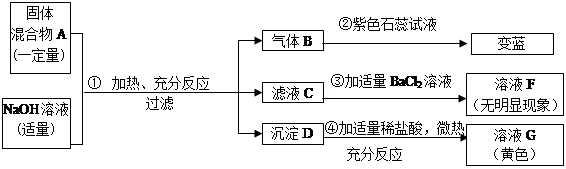
试根据实验过程和发生的现象填写以下空白:
(1)产生的气体B的化学式为。
(2)混合物A中,一定不存在的物质是原因是
(3)溶液F中含有的阳离子是(写离子符号)。
(4)写出实验过程④中发生化学反应的方程式。
三位同学用下图所示装置做一氧化碳还原氧化铁的实验。请帮他们写出一氧化碳还原氧化铁的化学方程式。当观察到玻璃管A中的粉末由红色逐渐变为黑色时,停止加热,继续通一氧化碳,冷却到室温,停止通气,同时观察到澄清的石灰水变浑浊。
用一氧化碳还原氧化铁的实验装置
小明认为:依据上述实验现象可以判断出生成的黑色固体为金属铁。
小红认为:仅从上述实验现象,不足以证明生成的黑色固体为金属铁,她增加了一个实验:用磁铁靠近生成的黑色固体,看到有黑色固体被磁铁吸引。于是得出生成的黑色固体为金属铁的结论。
小光通过查询有关资料得知:
(1)一氧化碳与氧化铁在加热条件下可能会生成四氧化三铁这种物质。
(2)四氧化三铁为黑色固体,有强磁性,也能够被磁铁吸引。
因此,小光认为小明和小红的结论都不能成立,你是否同意他的说法?,
请具体说明你的理由。
小光想通过实验检验生成的黑色固体是否含有金属铁。请你帮他完成实验并填写下表。
| 实 验 步 骤 |
实 验 现 象 |
实 验 结 论 |
| 取少量黑色固体于试管中,向其中滴加适量稀盐酸 |
① ②若没有气泡产生 |
①则黑色固体中含金属铁 ② |
(3)除上述方案,小光还想出了另外一种方案,他把少量黑色固体放入盛有硫酸铜溶液的试管中,通过观察,来判断黑色固体中是否含有金属铁;
请帮小光写出铁与硫酸铜溶液反应的化学方程式。