我国从1994年开始强制食盐加碘,即在食盐中加入碘酸钾(KIO3),以防治碘缺乏病的发生,今年将适当下调现行食盐加碘量。各地将根据本地区实际情况作相应调整。深圳已率先作出调整,由原来每千克食盐含碘40 mg下调至25 mg。
(1)碘酸钾中碘元素、钾元素、氧元素的质量比为______________;
(2)碘酸钾中碘元素的质量分数为_______;(保留至0.1%或用分数表示)
(3)请为我市某企业计算:售往深圳的加碘食盐每袋(500 g)应比调整前少加碘酸钾多少毫克。
某碳酸钠样品含有少量的硫酸钠,取一定质量的该样品,完全溶解在水中配制成
溶液,将其全部加入到
一定质量分数的硫酸溶液中,恰好完全反应,生成的气体全部逸出后,所得溶液质量是
,将溶液蒸干,得到
硫酸钠。
计算:
(1)加入的硫酸溶液的溶质质量分数;
(2)原碳酸钠样品中碳酸钠的质量分数(计算结果精确到0.1%)。
为测定某
溶液的溶质质量分数,用溶质质量分数为7.3%的稀盐酸进行滴定。现取待测液50.0 g,滴定过程如图所示。
(滴定反应为:
,
的相对原子质量为108,计算结果均保留1位小数)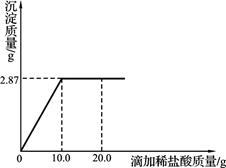
(1)
的相对分子质量为:;
(2)计算
溶液的溶质质量分数:;
(3)计算恰好完全反应时,所得溶液的溶质质量分数:。
请根据下图所示的实验过程和提供的数据计算:
(1)最终生成的不饱和溶液中溶质的质量为。
(2)合金中铜的质量分数;
(3)求所加稀硫酸的溶质质量分数。
(4)(1)配制本实验需要的稀硫酸,大斌选用的是98%的浓硫酸,请问在配制过程中需要另外加水多少克?
现有硫酸钠和硫酸镁固体混合物8 g,向其中加入一定量的氢氧化钠溶液恰好完全反应,过滤,得到2.9g沉淀和溶质质量分数为10 %的滤液。求:
(1)混合物中硫酸镁的质量分数;
(2)加入氢氧化钠溶液的溶质质量分数(计算结果精确到0.1%(。
某钢铁厂每天需消耗1000t含氧化铁80%的赤铁矿石,该厂理论上可以炼出含铁96%的生铁的质量是多少?