(12分)甲、乙、丙、丁四种物质均为下列离子组成的可溶性化合物,组成这四种物质的离子(离子不能重复组合)有:
| 阳离子 |
Ag+、Mg2+、Al3+、Ba2+ |
| 阴离子 |
Cl-、SO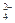 、NO3-、OH- 、NO3-、OH- |
现进行以下实验,
①将乙的溶液分别加到足量甲、丁两溶液中时均产生稳定的白色沉淀;
②将少量丙溶液滴入丁溶液时产生白色沉淀,当丙过量时沉淀完全溶解;
③甲、丙两溶液混合时产生的白色沉淀,经分析其中含有两种成份。
据此回答下列问题:
(1)写出电解质的化学式:甲 乙
(2)丙的阴离子的电子式是 ,丁的阳离子的结构示意图是 ;
(3)写出相应离子方程式:
①甲溶液与丙溶液混合:
②乙溶液与丁溶液混合: 
(1)和是衡量共价键稳定性的参数。
(2)键长是形成共价键的两个原子之间的间距。键长越长,键能(填“大”或“小”),键越断裂,化学性质越(填“稳定”或“不稳定”)。
(3)键角是描述的重要参数,分子的许多性质都与键角有关。CO2是形分子,键角。H2O是型分子,键角。
(1)原子轨道中相互重叠形成的和总称价键轨道,是分子结构的价键理论中最基本的部分。
(2)σ键强度π键(填“>”“〈”或“=”)
(3)σ键的特征是:以形成的两原子核的连线为轴作旋转操作,共价键的电子云。
按共价键的共用电子对理论,不可能有H3、H2Cl、和Cl3分子,这表明共价键具有。
PtCl2(NH3)2可以形成两种固体,一种为淡黄色,在水中的溶解度小,另一种为黄绿色,在水中的溶解度较大,请回答下列问题:
⑴PtCl2(NH3)2是平面正方形结构,还是四面体结构
⑵ 请在以下空格内画出这两种固体分子的几何构型图,淡黄色固体:,黄绿色固体:
⑶ 淡黄色固体物质是由分子组成,黄绿色固体物质是由分子组成(填“极性分子”或“非极性分子”)
⑷ 黄绿色固体在水中溶解度比淡黄色固体大,原因是
2003年10月16日“神舟五号”飞船成功发射,实现了中华民族的飞天梦想。
运送飞船的火箭燃料除液态双氧水外,还有另一种液态氮氢化合物。已知该化合物中氢元素的质量分数为12.5%,相对分子质量为32,结构分析发现该分子结构中只有单键。
(1)该氮氢化合物的电子式为。
(2)若该物质与液态双氧水恰好完全反应,产生两种无毒又不污染环境的气态物质,写出该反应的化学方程式。
(3)NH3分子中的N原子有一对孤对电子,能发生反应:NH3+HCl=NH4Cl。试写出上述氮氢化合物通入足量盐酸时,发生反应的化学方程式。