下列反应均为吸热反应,其中一定不能自发进行的是
A.(NH4)2CO3(s)=NH 4HCO3(s)+NH3(g) 4HCO3(s)+NH3(g) |
B.2N2O5(g)=4NO2(g)+O2(g) |
| C.MgCO3(s)=MgO(s)+CO2(g) | D.2CO(g)=2C(s)+O2(g) |
有A、B、C、D四种短周期元素在周期表中位置如图所示。
| …… |
C |
|||
| A |
B |
…… |
D |
已知:A2+与C原子的电子数相差2。下列推断不正确的是
A.A和D组成的化合物是弱电解质且水溶液呈酸性
B.与A同周期且与C同主族的E元素,其最高价氧化物对应水化物在某些化学反应中常作催化剂。
C.离子半径:C>A>B
D.B与C形成的化合物是冶金工业的一种原料
分子式为C9H12O属于芳香醇且苯环上有三个取代基的同分异构体共有
| A.4种 | B.5种 | C.6种 | D.8种 |
| …… |
C |
|||
| A |
B |
…… |
D |
化学与人类生活密切相关,下列与化学有关的说法不正确的是
| A.化石燃料燃烧和工业废气中的氮氧化物均是导致“雾霾天气”的元凶 |
| B.开发和推广新能源是实现低碳生活的途径之一 |
| C.粮食酿酒主要经过了淀粉→葡萄糖→乙醇的化学变化过程 |
| D.化学药品着火,都要立即用水或泡沫灭火器灭火 |
下表是25°C时某些盐的浓度积常数和弱酸的电离平衡常数,下列说法正确的是
| 化学式 |
AgCl |
Ag2CrO4 |
CH3COOH |
HClO |
H2CO3 |
| Ks或Ka |
Ksp=1.8×10-10 |
Ksp=2.0×10-12 |
Ka=1.8×10-5 |
Ka=3.0×10-8 |
Ka1=4.1×10-7 Ka2=5.6×10-11 |
A.相同浓度CH3COONa和NaClO的混合液中,各离子浓度的大小关系是c(Na+)>c(ClO-)>c(CH3COO-)>c(OH-)>c(H+)
B.向0.1mol·L-1CH3COOH溶液中滴加NaOH溶液至c(CH3COOH):c(CH3COO-)=5:9,此时溶液pH=5
C.碳酸钠溶液中滴加少量氯水的离子方程式为CO2-3 + Cl2+H2O =HCO-3+Cl-+HClO
D.向浓度均为1×10-3mol·L-1的KCl和K2CrO4混合液中滴加1×10-3mol·L-1的AgNO3溶液,CrO2-4先形成沉淀
电化学降解NO3-的原理如图所示。下列说法中正确的是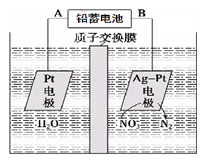
| A.铅蓄电池的A极为负极,电极材料为Pb |
| B.铅蓄电池工作过程中每通过电路中2mol电子则消耗1molH2SO4 |
| C.该电解池的阴极反应为2NO3- + 12H++ 10e- = N2↑ + 6H2O |
| D.若电解过程中转移5moL电子,则交换膜两侧电解液的质量变化差(Δm左—Δm右)为14.4g |