下列热化学方程式或离子方程式中,正确的是:
| A.将金属钠加入水中:2Na + 2H2O = 2Na+ + 2 OH- + H2↑ |
B.500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g) 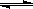 2NH3(g)△H= -38.6kJ·mol-1 2NH3(g)△H= -38.6kJ·mol-1 |
| C.甲烷的标准燃烧热为-890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为: CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H= -890.3kJ·mol-1 |
| D.氯化镁溶液与氨水反应:Mg2++2 OH-=Mg(OH)2 |
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
① CH3OH(g)+H2O(g)===CO2(g)+3H2(g) ΔH=+49.0 kJ/mol
② CH3OH(g)+1/2O2(g)===CO2(g)+2H2(g) ΔH=-192.9 kJ/mol
则下列说法不正确的是()
| A.CH3OH的燃烧热为192. 9 kJ/mol |
| B.CH3OH转变成H2的过程不一定要吸收能量 |
| C.根据①②推知反应:H2O(g)== H2(g) +1/2O2(g) ΔH=+241.9 kJ/mol |
| D.根据②推知反应:CH3OH(l)+1/2O2(g)===CO2(g)+2H2(g)的ΔH>-192.9 kJ/mol |
已知:①101 kPa时,2C(s)+O2(g)==="2CO(g)" ΔH=-221 kJ/mol
②稀溶液中,H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ/mol
下列结论正确的是()
| A.碳的燃烧热大于110.5 kJ/mol |
| B.①的反应热为221 kJ/mol |
| C.稀硫酸与稀NaOH溶液反应的中和热为-57.3 kJ/mol |
| D.浓硫酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ热量 |
设反应①Fe(s)+CO2(g) FeO(s)+CO(g) ΔH=a kJ·mol-1,
FeO(s)+CO(g) ΔH=a kJ·mol-1,
反应②Fe(s)+H2O(g) FeO(s)+H2(g) ΔH=b kJ·mol-1,以上两反应的平衡常数分别为
FeO(s)+H2(g) ΔH=b kJ·mol-1,以上两反应的平衡常数分别为
K1和K2,在不同温度下,K1、K2的值如下:
| T/K |
K1 |
K2 |
| 973 |
1.47 |
2.38 |
| 1 173 |
2.15 |
1.67 |
下列有关叙述正确的是( )
A.b>0 B.在973 K下增大压强,K2增大
C.a>b D.在常温下反应①一定能自发进行
对于可逆反应2AB3(g) 2A(g) + 3B2(g) △H>0,下列图像不正确的是( )
2A(g) + 3B2(g) △H>0,下列图像不正确的是( )
已知:25 ℃时,Mg(OH)2的Ksp=5.61×10-12,MgF2的Ksp=7.42×10-11。下列判断正确的是()
A.25 ℃时,饱和Mg(OH)2溶液与饱和MgF2溶液相比,前者的c(Mg2+)大
B.25 ℃时,在Mg(OH)2的悬浊液中加入少量的NH4Cl固体,c(Mg2+)增大
25 ℃时,Mg(OH)2固体在20 mL 0.01 mol/L的氨水中的Ksp比在20 mL 0.01 mol/L NH4Cl溶液中的Ksp小
D.25 ℃时,在Mg(OH)2的悬浊液中加入NaF溶液后,Mg(OH)2不可能转化为MgF2