南宁至钦州段的高速铁路正在建设中。请回答下列问题:
(1)铁路建设中大量使用了以下材料:①石子;②钢筋水泥柱;③钢轨等,其中钢轨属于。
| A. | 金属材料 | B. | 合成材料 | C. | 有机天然材料 | D. | 无机非金属材料 |
(2)建设中,常用铝和氧化铁(
)在高温条件下,反应生成熔融状态下的铁单质对钢轨中的缝隙进行焊接。反应的化学方程式为:
,则
的化学式为,该反应的基本类型是。
(3)钢轨长时间使用后会生锈。铁锈的主要成分是
;除铁锈常用的一种试剂是。
(4)请写出防止铁制品锈蚀的两种常用方法:①;②。
回答下列与含碳物质有关的问题。
(1)天然存在的最硬的物质是 ;
(2)能将 CO 和 CO 2鉴别开的溶液是 ;
(3)K 2CO 3、Na 2CO 3、NaHCO 3都能与 (填具体物质)反应,生成CO 2。
结合如图所示实验,回答有关问题。

(1)实验一的目的是 ;
(2)实验二的结论:铁生锈是铁与 共同作用的结果;
(3)实验三,在B试管加入 (写出一种情况),即可证明温度和固体颗粒大小都是影响冰糖溶解快慢的因素。
回答下列与水有关的问题.
(1)利用 的吸附性去除水中的异味;
(2)生活中可通过 方法降低水的硬度;
(3)在电解水实验中, 极产生的气泡能够燃烧.
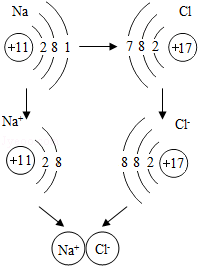
如图是金属钠与氯气反应生成氯化钠的微观示意图,根据图示回答下列问题。
(1)钠原子的最外层电子数为 ;
(2)构成氯化钠的粒子是 ;
(3)由原子核外电子层数与元素所在周期表中的周期数相同可知,氯元素在元素周期表中应排在第 周期。
回答下列问题.
(1)氧元素的符号是 ;
(2)3个氢原子可表示为 ;
(3)生理盐水中溶剂的化学式为 .