检验某未知溶液中是否含有SO42-,下列操作最合理的是 ( )
| A.加入稀硝酸酸化的Ba(NO3)2溶液 |
| B.加入盐酸酸化的BaCl2溶液 |
| C.先加稀硝酸酸化,再加Ba(NO3)2溶液 |
| D.先加盐酸酸化,再加BaCl2溶液 |
下列说法正确的是
| A.直径介于1 nm~100 nm之间的微粒称为胶体 |
| B.制备Fe(OH)3胶体的方法是将饱和FeCl3溶液加热煮沸 |
| C.胶体与浊液的本质区别是其稳定性,胶体属于介稳体系 |
| D.利用丁达尔效应可以区分溶液和胶体溶液 |
下列物质之间的反应,一定不能生成盐的是
| A.酸性氧化物与碱反应 | B.碱性氧化物与酸反应 |
| C.金属与氧气化合 | D.单质与化合物的置换反应 |
盛放浓硫酸的试剂瓶的标签上印有下列警示标记中的
 |
 |
 |
 |
| A |
B |
C |
D |
某温度时,在密闭容器中,X、Y、Z三种气体浓度的变化如图Ⅰ所示,若其它条件不变,当温度分别为T1和T2时,Y的体积分数与时间关系如图Ⅱ所示。则下列结论正确的是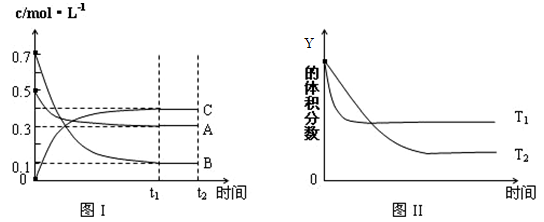
A.该反应的热化学方程式为:X(g)+3Y(g) 2Z(g);△H<0 2Z(g);△H<0 |
| B.若其它条件不变,升高温度,正、逆反应速率均增大,X的转化率增大 |
| C.达到平衡后,若其他条件不变,减小体积,平衡向逆反应方向移动 |
| D.达到平衡后,若其他条件不变,通入稀有气体,平衡向正反应方向移动 |
反应N2O4(g) 2NO2(g) △H=+57kJ/mol,在温度T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示。下列说法正确的是
2NO2(g) △H=+57kJ/mol,在温度T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示。下列说法正确的是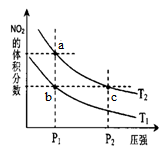
| A.a、c两点的反应速率:a>c |
| B.a、c两点气体的颜色:a浅,c深 |
| C.a、b两点气体的平均相对分子质量:a>b |
| D.b、c两点化学平衡常数:b<c |