下列实验操作中正确的是
| A.蒸馏操作时,应向蒸馏液体中加入几块沸石,以防止暴沸 |
B.蒸发操作时 ,应使混合物中的水分完全蒸干后,才能停止加热 ,应使混合物中的水分完全蒸干后,才能停止加热 |
| C.分液操作时,先将分液漏斗中下层液体从下口放出,再将上层液体从下口放出 |
| D.萃取操作时,可以选用CCl4或酒精作为萃取剂从溴水中萃取溴 |
| A.碳酸氢钙溶液跟稀硝酸反应 HCO 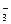 +H+===H2O+CO2↑ +H+===H2O+CO2↑ |
| B.饱和石灰水跟稀硝酸反应 Ca(OH)2+2H+===Ca2++2H2O |
| C.向稀氨水中加入稀盐酸 NH3·H2O+H+===NH 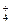 +H2O +H2O |
| D.碳酸钙溶于醋酸中 |
CaCO3+2H+===Ca2++H2O+CO2
| A.向氢氧化钠溶液中通入少量CO2 OH-+CO2===HCO  |
| B.用氨水吸收少量SO2 2NH3·H2O+SO2===2NH  +SO +SO +H2O +H2O |
| C.硝酸铝溶液中加入过量氨水 Al3++4NH3·H2O===AlO  +4NH +4NH +2H2O +2H2O |
| D.向Fe2(SO4)3的酸性溶液中通入足量H2S |
Fe3++H2S===Fe2++S↓+2H+
| A.向碳酸氢钙溶液中加入过量氢氧化钠 Ca2++2HCO  +2OH-===CaCO3↓+2H2O+CO +2OH-===CaCO3↓+2H2O+CO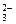 |
| B.等体积等物质的量浓度的氢氧化钡溶液与碳酸氢铵溶液混合 Ba2++2OH-+NH  +HCO +HCO ===BaCO3↓+NH3·H2O+H2O ===BaCO3↓+NH3·H2O+H2O |
| C.氢氧化铝与足量盐酸反应 Al(OH)3+3H+===Al3++3H2O |
| D.过量CO2通入氢氧化钠溶液中 |
CO2+2OH-===CO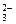 +H2O
+H2O
A.H3O+、NO 、Fe2+、Na+ 、Fe2+、Na+ |
B.Ag+、NO 、Cl-、K+ 、Cl-、K+ |
C.K+、Ba2+、OH-、SO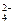 |
D.Cu2+、NH 、Br-、OH- 、Br-、OH- |
| A.碳酸钙与醋酸 CaCO3+2H+===Ca2++CO2↑+H2O |
| B.澄清石灰水中加入盐酸 Ca(OH)2+2H+===Ca2++2H2O |
| C.铜片加入稀硝酸中 Cu+NO  +4H+===Cu2++NO↑+2H2O +4H+===Cu2++NO↑+2H2O |
| D.小苏打溶液和甲酸混合 |
HCO +HCOOH===HCOO-+CO2↑+H2O
+HCOOH===HCOO-+CO2↑+H2O